医耘沙龙第五期-临床CRO行业报告与投资机会探讨
来源:华医资本 2019-10-21 17:04
2019年10月17日“医耘沙龙”第五期临床CRO投资研究主题深度沙龙如期举行,本次沙龙由华医资本旗下医耘资本、胡润百富、生物谷以及杭州银行联合筹备,邀请了华医资本创始合伙人刘云博士,方恩医药高级副总裁傅维明博士以及有临医药联合创始人谭青乔博士对临床CRO行业从发展、最新政策解读以及未来发展趋势等角度进行了深度探讨,数十位投资人参与讨论。核心要点:1.国内迎来创新药浪潮,看好临床CRO行业。2.临
2019年10月17日“医耘沙龙”第五期临床CRO投资研究主题深度沙龙如期举行,本次沙龙由华医资本旗下医耘资本、胡润百富、生物谷以及杭州银行联合筹备,邀请了华医资本创始合伙人刘云博士,方恩医药高级副总裁傅维明博士以及有临医药联合创始人谭青乔博士对临床CRO行业从发展、最新政策解读以及未来发展趋势等角度进行了深度探讨,数十位投资人参与讨论。
核心要点:
1.国内迎来创新药浪潮,看好临床CRO行业。
2.临床CRO中,具有国际化创新药临床能力的CRO会快速发展。
3.考察创新药CRO企业需要重点关注阶段、目前项目经验、团队能力、运营能力和资本运作能力。
1.CRO的定义和市场现状
CRO(Clinical Research Organization,合同研究组织)主要为制药公司提供药物发现、临床前研究、临床试验等合同研究服务。
按照服务的阶段不同可以将医药CRO分为临床前CRO和临床CRO,在各阶段医药CRO承担的任务不同。临床阶段CRO主要提供Ⅰ~Ⅳ期临床试验技术服务、临床试验数据管理和统计分析、注册申报以及上市后药物安全监测等。
图1:临床CRO的分类
数据来源:公开资料,华医资本整理
由于医药研发投入高、周期长、风险大,及临床试验业务繁、费用高、周期长等原因,CRO的渗透率正在逐年上升。根据南方所的数据,目前我国医药CRO行业正处于快速发展期,市场规模已由2011年的140亿元,增长至2018年的678亿元,预计2021年将达到1154亿。
图2:我国临床CRO的增速
数据来源:南方所,华医资本整理
然而,我们也看到这样一个现象,国际临床CRO市场规模占到国际CRO市场规模的82%,而中国临床CRO市场规模仅占整个中国CRO市场规模的57%。
图3:中国与国际医药CRO市场业务占比
数据来源:Clinical Leader,华医资本整理
这里面的原因也可想而知,中国的CRO成长史和药物早期开发有着密切的关系。国内成立的CRO,最初就是专门从事化合物人工合成的。这项工作基本上是项海底捞针,需要投入大量人力来化学合成无数的化合物。国外很多企业来找中国CRO企业做化合物合成,后续化合物的具体筛选、活性测试等方面都交给国外药企自己做。这个阶段很多临床前CRO得到快速发展,比如2000年药明康德成立,2003年睿智化学成立,2003年美迪西成立,2004年康龙化成成立,2004年桑迪亚成立的。
而临床CRO,由于具有地域限制,国内的CRO很难做跨国的订单(除了数据管理),再加上国内前十几年需求主要是仿制药的BE为主,总体来说订单量小,难度低。
因此,虽然中国临床CRO自2000年之后也快速成长,但是整体来说服务质量和国外CRO还有差距。竞争格局而言,虽然目前国内有500多家CRO,但是本土大型CRO并不多。
图4:中国临床CRO竞争格局
数据来源:泰格医药招股说明书,华医资本整理
那么接下去临床CRO的发展趋势如何?这是我们本篇报告的关注重点。
2.临床CRO新变量和新挑战
说到临床CRO的发展趋势,我们就要看药企的研发策略。而药物的研发策略的调整,又与中国本土政策环境的变化息息相关。
一方面我们可以看到,由于一致性评价,专做仿制药的CRO在2017和2018年有了一波强劲的增长,然而就目前来看持续增长也遇到瓶颈期。举例来说,面对这两年的“4+7”,许多企业开始放弃仿制药管线;另外BE的执行难度又低于创新药,很难直接形成很强的竞争优势。就华医研究院了解,目前很多仿制药CRO都在谋求从仿制药向新药CRO的转型。
另一方面,优先审评审批制度的落地、上市许可持有人制度的实施和加入ICH等一系列政策与举措,正在驱动越来越多的中国药企走出国门,也会有越来越多的国外药企走入中国。这些创新药需求也在拉动着创新药CRO的增长。
就拿2017年中国加入ICH来举例。中国加入ICH,标着着中国新药研发数据和注册的国际互认,利好国际药企(MNC)在中国做MRCT,也激励着中国的创新药走向世界。
然而对于创新药公司来说,这些是利好也是挑战,需要有经验的CRO一起协同。举例来说,本土创新药企业如何与FDA和中国NMPA同时召开pre-IND会议,以设计在两个市场均适用的临床和监管策略?如何与在这两个国家/地区开展试验,设计受试者的分配以实现速度最大化并降低成本? 同时提供美国,中国和其他主要监管机构所需的数据?
走向国内的国际药企也是如此,哪里有资源可以桥接中国和外国临床开发领域和监管细微差别的了解不足?是否会因此产生很多管理方面的干扰?是否可以确定来自中国的数据质量能够支持他们的全球计划并达到关键的里程碑?
因此我们可以看到,对于国际化、创新药临床CRO的需求正在增加。因此我们认为创新药CRO机会实现高速发展。
3.我们看好的创新药CRO是怎么样的?
那么好的创新药CRO具有怎么样的特点呢?
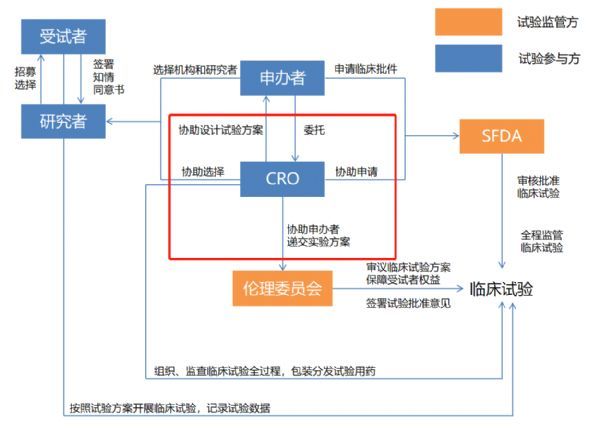
首先临床CRO是服务型行业,从下图可以看出一个临床试验需要多领域的配合,医生、患者、监管当局、临床中心、支付方和CRO的合作决定了临床开发的质量。
图5:临床CRO在临床试验的角色
数据来源:公开资料,华医资本整理
其次新药临床试验非常专业。临床试验的目的是在人的身上研究和证明,找到最合适的剂量,对新药的安全性、有效性进行评估。因此新药临床CRO需要的人才多而专业,包括临床科学家,临床药理学家,生物统计学家, 药物安全和风险管理专家,以及境内外注册专家。
综上所述,我们判断创新药临床CRO会越来越趋向于专业化。
服务+专业是执行一个好订单的基础,那么这套机制运作起来,我们就以华医药资本的IP “大白“ 来比喻我们看好的CRO:左手能获得并筛选优质订单,大脑能进
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->