卵巢癌重磅!阿斯利康/默沙东Lynparza(利普卓)+贝伐单抗一线维持治疗2年无进展生存率达46%
来源:本站原创 2019-09-30 11:46
2019年09月30日讯 /生物谷BIOON/ --2019年欧洲肿瘤医学学会(ESMO)年会于9月27日至10月1日在西班牙巴塞罗那举行。此次会议上,阿斯利康(AstraZeneca)和默沙东(Merck & Co)公布了Lynparza(中文品牌名:利普卓,通用名:olaparib,奥拉帕利片剂)治疗卵巢癌III期临床研究PAOLA-1的详细积极数据。PAOLA-1是一项双盲研究,在接

2019年09月30日讯 /生物谷BIOON/ --2019年欧洲肿瘤医学学会(ESMO)年会于9月27日至10月1日在西班牙巴塞罗那举行。此次会议上,阿斯利康(AstraZeneca)和默沙东(Merck & Co)公布了Lynparza(中文品牌名:利普卓,通用名:olaparib,奥拉帕利片剂)治疗卵巢癌III期临床研究PAOLA-1的详细积极数据。
PAOLA-1是一项双盲研究,在接受含铂化疗和Avastin(贝伐单抗)一线治疗病情获得完全缓解或部分缓解的新诊晚期FIGO III-IV期高级别浆液性或子宫内膜样卵巢、输卵管或腹膜癌患者中开展,评估了Lynparza与标准护理(SoC)贝伐单抗联合治疗相对于贝伐单抗单药疗法用作一线维持治疗的疗效和安全性。结果显示,用于一线维持治疗时,与贝伐单抗单药治疗相比,Lynparza与贝伐单抗联合治疗使无进展生存期(PFS)取得了统计学意义和临床意义的改善,不论患者的基因生物标志物状态或先前手术结果如何。
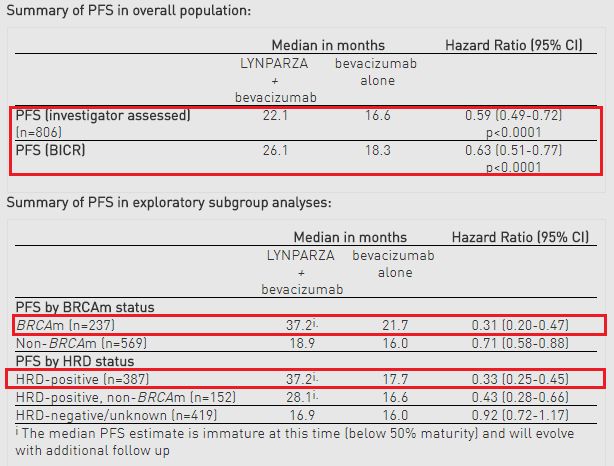
具体数据为:调查员评估的结果显示,与贝伐单抗单药治疗组相比,Lynparza+贝伐单抗联合治疗组疾病进展或死亡风险将更低41%(HR=0.59)、疾病无进展生存期显著延长(22.1个月 vs 16.6个月)。在研究开始后的2年时间点,Lynparza+贝伐单抗联合治疗有46%的患者没有疾病进展,而贝伐单抗单药治疗组比例为28%。盲法独立中心审查(BICR)的PFS敏感性分析结果一致,显示出类似的改善:Lynparza+贝伐单抗联合治疗组中位PFS为26.1个月,贝伐单抗单药治疗组为18.3个月。该研究中,Lynparza和贝伐单抗的安全性及耐受性与之前每种药物的研究结果一致,对生活质量没有损害。
该研究还包括探索性分组分析,包括BRCA突变(BRCAm)和更广泛的同源重组缺陷(HRD)群体,结果显示,与贝伐单抗单药治疗相比,Lynparza+贝伐单抗联合治疗显示更大的治疗受益。在BRCAm阳性亚组中,Lynparza+贝伐单抗联合治疗疾病进展或死亡风险降低69%(HR=0.31,中位PFS:37.2个月 vs 21.7个月)。在更广泛的HRD阳性亚组(约占新诊晚期卵巢癌女性患者病例的一半,包括BRCAm)中,Lynparza+贝伐单抗联合治疗将疾病进展或死亡风险降低了67%(HR=0.33,中位PFS:37.2个月 vs 17.7个月)。
值得一提的是,PAOLA-1研究是涉及Lynparza一线维持治疗晚期卵巢癌方面的第二项阳性III期研究。此前,来自关键性III期研究SOLO-1的数据显示,在接受一线含铂化疗病情处于完全缓解或部分缓解的BRCA突变(BRCAm,生殖系和/或体细胞)晚期(FIGO分期:III期和IV期)卵巢癌患者中,与安慰剂相比,Lynparza一线维持治疗将疾病进展或死亡风险显著降低70%(HR=0.30,p<0.001)。随访41个月,Lynparza治疗组中位无进展生存期(PFS)尚未达到,安慰剂组为13.8个月。Lynparza治疗组有60.4%的患者在治疗36个月内病情没有进展,安慰剂组为26.9%。该研究中,Lynparza的安全特征与之前的研究一致。
阿斯利康肿瘤研发执行副总裁Jos é Basegga表示:“这项研究旨在反映使用一种全球标准护理药物贝伐单抗与Lynparza联合用药的日常临床实践。结果显示,在两年内,Lynparza联合贝伐单抗一线维持治疗的晚期卵巢癌患者中有近一半患者疾病没有进展,不轮其生物标志物状态或手术结果如何。我们我们正与监管机构合作,尽快将Lynparza带给这些患者。”
默沙东全球临床开发负责人、高级副总裁兼默沙东研究实验室首席医疗官Roy Baynes表示:“PAOLA-1研究是涉及Lynparza一线维持治疗晚期卵巢癌方面的第二个阳性III期研究。继阳性SOLO-1研究之后,我们对PAOLA-1研究的结果感到鼓舞,该研究重申了阿斯利康和默沙东探索潜在治疗方案用于更多卵巢癌女性患者的持续承诺。”
PAOLA-1研究的首席调查员、法国国家卵巢癌调查研究组织(GINECO)总裁、法国里昂莱昂•贝拉尔(Léon Bérard)癌症治疗中心肿瘤内科医师Isabelle Ray Coquard表示:“对新诊断为晚期卵巢癌的女性进行一线治疗(包括维持治疗)的目标是延缓复发。不幸的是,复发的风险仍然很高,有三分之二的女性在最初确诊后的三年内复发。PAOLA-1研究中,将Lynparza添加至标准护理药物贝伐单抗的治疗效果显著,有可能改变晚期卵巢癌女性患者一线维持治疗的临床实践。”
Lynparza是一种首创、口服多聚ADP核糖聚合酶(PARP)抑制剂,可利用肿瘤DNA损伤修复(DDR)通路的缺陷优先杀死癌细胞,这种作用模式赋予了Lynparza治疗存在DNA损伤修复缺陷的广泛类型肿瘤的潜力。
Lynparza是全球上市的首个PARP抑制剂,于2014年12月首次获美国FDA批准。截至目前,该药已获全球64个国家批准,用于维持治疗铂敏感复发性卵巢癌(不论BRCA状态如何)。该药在美国、欧盟、日本和其他一些国家被批准作为一线维持疗法,用于含铂化疗后病情缓解的BRCA突变(BRCAm)晚期卵巢癌。此外,在包括美国和日本在内43个国家还被批准用于先前接受过化疗的生殖系BRCAm HER2阴性转移性乳腺癌,在欧盟,该适应症包括局部晚期乳腺癌。目前,Lynparza治疗卵巢癌、乳腺癌、胰腺癌正在接受其他管辖区域的审查。
阿斯利康与默沙东于2017年7月达成肿瘤学全球战略合作,共同开发和商业化Lynparza及另一种MEK抑制剂selumetinib治疗多种类型肿瘤。在PARP抑制剂范畴,Lynparza拥有最广泛和最先进的临床试验开发项目。目前,双方正在合作,调查Lynparza作为单药疗法以及组合疗法用于广泛类型肿瘤的治疗潜力。
在中国市场,Lynparza(利普卓)于2018年8月获批,用于铂敏感复发性卵巢癌的维持治疗。Lynparza是中国市场首个获批治疗卵巢癌的靶向药物,标志着中国卵巢癌治疗进入PARP抑制剂时代。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


