2019年8月Science期刊不得不看的亮点研究
来源:本站原创 2019-08-31 23:57
2019年8月31日讯/生物谷BIOON/---2019年8月份即将结束了,8月份Science期刊又有哪些亮点研究值得学习呢?小编对此进行了整理,与各位分享。1.Science:重大突破!CRISPR-Cas系统新用途!开发出可编程的CRISPR反应性智能材料doi:10.1126/science.aaw5122; doi:10.1126/science.aay4198CRISPR-Cas系统已
2019年8月31日讯/生物谷BIOON/---2019年8月份即将结束了,8月份Science期刊又有哪些亮点研究值得学习呢?小编对此进行了整理,与各位分享。
1.Science:重大突破!CRISPR-Cas系统新用途!开发出可编程的CRISPR反应性智能材料
doi:10.1126/science.aaw5122; doi:10.1126/science.aay4198
CRISPR-Cas系统已成为科学家们在不断增加的有机体中研究基因的首选工具,并且正被用于开发潜在地校正基因组中单个核苷酸位点上的缺陷的新型基因疗法。它也被用于正在进行的诊断方法中,用于检测患者体内的病原体和致病突变。
如今,在一项新的研究中,来自美国哈佛大学威斯生物启发工程研究所和麻省理工学院的研究人员展示了将CRISPR用作新型刺激反应性“智能(smart)”材料的控制元件。一旦被特定的天然的或用户定义的DNA刺激物激活,一种CRISPR-Cas酶就能够让多种智能材料释放出自身结合的货物,比如染料和活性酶,改变它们的结构来部署包埋的纳米颗粒和活细胞,或者调节电路从而将生物信号转化为电信号。相关研究结果发表在2019年8月23日的Science期刊上,论文标题为“Programmable CRISPR-responsive smart materials”。

论文通讯作者、哈佛大学威斯生物启发工程研究所创始核心学院成员James Collins博士说,“我们的研究表明CRISPR的力量可以在实验室之外用于控制DNA反应性材料的行为。我们开发了一系列具有不同能力的材料,这就突显了可编程的CRISPR反应性智能材料(CRISPR-responsive smart material)所支持的应用范围。这些应用包括新型治疗诊断策略、即时诊断以及对流行病爆发和环境危害进行的区域监测。”
论文共同第一作者、麻省理工学院研究生Max English说,“我们将单链靶DNA序列整合到聚合物材料中,要么作为悬垂货物的锚点,要么作为维持材料基本完整性的结构元件,并且能够通过提供Cas12a和一种作为刺激物的特定gRNA来控制不同的材料行为。”
2.Science:构建出疟原虫完整生命周期的细胞图谱---疟疾细胞图谱,极大加快疟疾研究和疗法开发
doi:10.1126/science.aaw2619; doi:10.1126/science.aay5963
在一项新的研究中,来自英国、丹麦、肯尼亚、南非、澳大利亚、瑞典和法国的研究人员构建出疟疾细胞图谱(Malaria Cell Atlas),这种图谱呈现出疟原虫在所有形态生命周期阶段的转录组学特征。这种图谱的目标是(i)了解在整个生命周期中的基因功能和使用;(ii)理解发育阶段转变背后的基因调控机制;(iii)发现疟原虫两头下注(bet-hedging)模式;(iv)提供一种参考数据集,可用于了解多种疟原虫物种在实验室中和在自然感染下的寄生虫生物学特性。相关研究结果发表在2019年8月23日的Science期刊上,论文标题为“The Malaria Cell Atlas: Single parasite transcriptomes across the complete Plasmodium life cycle”。
这些研究人员通过使用细胞分选方法分离出1787个疟原虫,并且在涵盖蚊子和哺乳动物宿主中所有生命周期阶段的10个时间点对它们的全长转录组进行了分析。
从这些数据中,他们能够了解发育的精细转录模式,并确定与疟原虫阶段、细胞策略(增殖阶段、生长阶段和有性阶段)和宿主环境相关的标志基因。对整个生命周期中的单细胞基因表达模式的比较揭示出在发育过程中有几组基因的表达模式相似。由此产生的行为相似的基因簇能够推断出仍然未被表征的大约40%基因的可能功能。
通过使用液滴测序,这些研究人员对来自三种疟原虫物种(包括两种人类疟原虫病原体)的红细胞内发育周期的另外15858个细胞进行了测序。他们在生命周期的致病阶段对这三种疟原虫物种的发育轨迹进行了比对,并建立了一种跨物种比较的方法。最后,他们开发出一种保存从天然的受感染携带者中收集的野生疟原虫的实验方案,使用scRNA-seq进行测序,并将疟疾细胞图谱作为参考,以便鉴定出野生疟原虫发育阶段并在单细胞分辨率下表征天然的混合物种感染。
3.Science:植物免疫系统新突破!揭示植物TIR结构域是一种促进细胞死亡的NAD+切割酶
doi:10.1126/science.aax1771
在一项新的研究中,一组研究人员阐明了植物免疫反应的一个关键方面。他们的发现揭示了植物抗性蛋白如何引发局部的细胞死亡,这可能导致人们在下一代作物中开发出进行抗病性改造的新策略。相关研究结果发表在2019年8月23日的Science期刊上,论文标题为“TIR domains of plant immune receptors are NAD+-cleaving enzymes that promote cell death”。论文通讯作者为科罗拉多州立大学生物学助理教授Marc Nishimura、北卡罗来纳大学教堂山分校的Jeff Dangl和华盛顿大学医学院的Jeffrey Milbrandt。
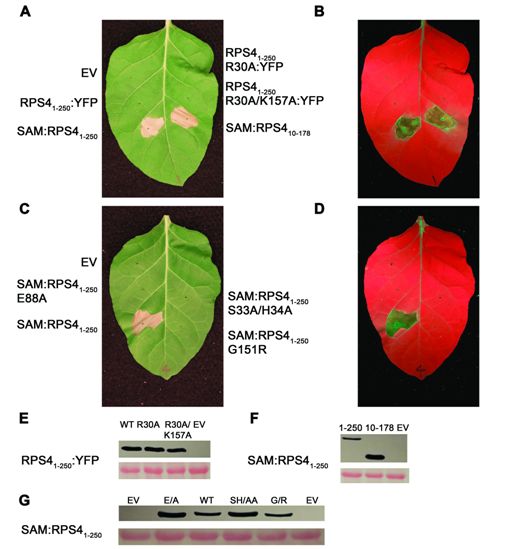
Nishimura与其同事们一起鉴定出植物抗性蛋白TIR的一种鲜为人知的结构域(即TIR结构域)的作用机制。他们发现在植物免疫反应期间,这种TIR结构域是一种降解NAD+分子的酶,其中NAD+分子对所有生物的新陈代谢至关重要。通过切割NAD+,植物自我破坏受感染的细胞,同时不会伤害其他未被感染的细胞。
在2017年,Nishimura在华盛顿大学医学院的合作者在一种名为SARM1的蛋白中观察到一种不寻常的动物TIR结构域,它不同于动物细胞中的其他TIR信号支架。相反,它作为一种酶发挥作用。Nishimura及其同事们开始探究这种结构域是否在植物免疫系统中发挥着具有类似的功能。
在这项新的研究中,Nishimura及其同事们发现TIR结构域在植物免疫反应中的作用确实与SARM1中功能上更不寻常的这种动物TIR结构域的作用相关。他们发现植物TIR结构域本身就是一种切割NAD+的酶,而不是作为招募其他成分的结构支架起作用。但是还存在一个重要的区别。虽然SARM1中的动物TIR结构域通过消耗NAD+水平来杀死细胞,但植物TIR结构域似乎切割NAD+来产生信号分子。这种并未在动物细胞中观察到的信号分子在结构上一种与称为环状ADP-核糖(cyclic ADP-Ribose)的经典信号分子有关。他们如今正在努力了解他们观察到的这种新产物如何影响细胞死亡和抗病能力。
4.Science:打破教科书! 皮肤中发现新的疼痛器官!
doi:10.1126/science.aax6452; doi:10.1126/science.aay6144
瑞典卡罗林斯卡学院的研究人员发现了一种新的感觉器官,它可以检测到疼痛的机械损伤,比如刺痛和撞击。这项发现发表在《Science》杂志上。
疼痛造成痛苦,并给社会带来巨大的经济损失。几乎每五个人中就有一个人经历持续的疼痛,因此很有必要寻找新的止痛药物。然而,对疼痛的敏感也是生存所必需的,它具有保护功能。它能促进防止损伤组织的反射反应,比如当你感到被尖锐物体刺痛或烧伤时把手抽离。
卡罗林斯卡学院的研究人员现在在皮肤上发现了一种新的感觉器官,它对有害的环境刺激很敏感。它由神经胶质细胞组成,有多个长长的突起,共同构成皮肤内网状的器官。这个器官对刺痛和压力等痛苦的机械损伤很敏感。
这项研究描述了新的痛觉器官的特点--它是如何与皮肤中的痛觉神经组织在一起的,以及该器官的激活如何导致神经系统中的电脉冲,从而导致反射反应和疼痛体验。组成器官的细胞对机械刺激高度敏感,这就解释了它们如何参与检测疼痛的针刺和压力。在实验中,研究人员还阻断了该器官的活动,从而导致机械疼痛的感觉能力下降。
5.Science重大突破:肠道细菌竟然可以预防肥胖!
doi:10.1126/science.aat9351
犹他大学健康学院的研究人员发现,肠道中有一种特定的细菌可以防止老鼠变胖,这表明这些细菌也可以控制人类的体重。这种有益的细菌被称为梭状芽孢杆菌(Clostridia),是微生物群落的一部分--肠道内共有数万亿的细菌和其他微生物。
近日发表在《Science》杂志上的这项研究表明,健康的老鼠体内有大量梭状芽孢杆菌(一种由20到30种细菌组成的细菌),但那些免疫系统受损的老鼠随着年龄的增长会失去这些微生物。即使喂食健康的食物,老鼠也不可避免地会变胖。把这类微生物还给这些动物可以让它们保持苗条。
这项研究的结果已经指向这个方向。Petersen和他的同事发现梭状芽孢杆菌通过阻断肠道吸收脂肪的能力来防止体重增加。实验中,梭状芽孢杆菌是小鼠肠道中唯一的细菌,与完全没有微生物群的小鼠相比,梭状芽孢杆菌的小鼠更瘦,脂肪更少。他们还拥有较低水平的CD36基因,该基因控制着身体对脂肪酸的吸收。
Round说,这些发现可能会导致一种治疗方法,它比粪便移植和益生菌更有优势--目前正被广泛研究作为恢复健康微生物群的方法。基于将活菌群转移到肠道的治疗方法并不适用于所有人,因为不同的饮食和其他因素会影响哪些细菌能够存活和繁殖。
6.Science:操纵蛋白GPR139有望更安全地使用阿片类药物
doi:10.1126/science.aau2078
在一项新的研究中,来自美国斯克里普斯研究所和堪萨斯大学的研究人员发现一种蛋白有朝一日可能经操纵后使得疼痛患者更安全地使用阿片类药物。相关研究结果于2019年8月15日在线发表在Science期刊上,论文标题为“Genetic behavioral screen identifies an orphan anti-opioid system”。
阿片类药物是一类用于减轻疼痛的药物,但是它们也很容易上瘾。不幸的是,科学家们一直无法找到阿片类药物的替代品,因此有些人已开始寻找让现有药物不那么容易上瘾的方法。在这项新的研究中,这些研究人员研究了通过遗传手段改变线虫以减少阿片类药物成瘾的方法。
这项研究涉及在线虫基因中产生900多种突变,然后对每种突变进行测试以便观察它是否导致对阿片类药物敏感性的任何变化。他们报道他们在一个称为FRPR-13的基因中发现了一种似乎可以减轻症状的突变。他们接下来在哺乳动物中发现FRPR-13同源基因,这个同源基因编码一种称为GPR139的蛋白。他们发现这种蛋白对μ-阿片受体(mu-opioid receptor, MOR)信号转导产生抑制作用。他们随后将注意力转向这个基因和这种蛋白在小鼠中的作用。他们的一项测试涉及通过遗传手段改变小鼠,从而阻止GPR139编码,这接着会阻止这种蛋白的产生。他们发现,这样做往往会增强阿片类药物(吗啡)抑制神经元放电的能力--- MOR水平下降了。最终结果就是疼痛减轻了。但是,测试还表明阻止GPR139产生导致成瘾小鼠出现更少的断瘾症状。
这些研究人员指出断瘾症状的减少可能是由于蓝斑核(locus coeruleus)中的神经元放电变化,其中蓝斑核是大脑的一部分,之前的研究表明它参与处理断瘾信号。他们最后建议GPR139有朝一日可以在减少人类患者的断瘾症状方面发挥重要作用,这会让阿片类药物变得更安全。
7.Science:受控的水力压裂让哺乳动物胚胎发育成形
doi:10.1126/science.aaw7709; doi:10.1126/science.aay2860
水力压裂(hydraulic fracturing)是一种最为常见的与页岩气开采相关的过程。在一项新的研究中,来自法国索邦大学居里研究所和法兰西学院生物跨学科研究中心的研究人员作出结论:自我压裂(self-fracking)是将胚胎(来自小鼠)从径向对称的细胞聚集体切换到双侧对称的囊胚(blastocyst)的机制。相关研究结果近期发表在Science期刊上,论文标题为“Hydraulic fracturing and active coarsening position the lumen of the mouse blastocyst”。
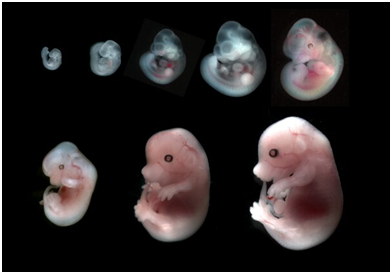
在植入之前,胚胎是一组紧密的细胞,这些细胞或多或少地径向分裂,因而大体上保持球形。随后,这些细胞变成两侧对称的囊胚---由充满液体的囊胚腔(blastocoel)、最终成为胎儿的内胚细胞团和最终变成胎盘的滋养外胚层(trophectoderm)组成。水力压裂发生在这两个步骤之间的过渡阶段;它是这些细胞如何沿着第一轴将它们的排列从径向对称切换到两侧对称。
通过使用高分辨率实时成像,这些研究人员观察到在小鼠囊胚形成过程中这种对称性破裂的过程。像往常一样,受精卵(精子和卵细胞结合形成的一个细胞)经细胞分裂后产生两个细胞,然后是四个,依此类推,直到第五轮细胞分裂,这时他们观察到“处数百个气泡在细胞-细胞连接处同步出现”,每个气泡充满着加压水。在这些气泡(微腔)的形成过程中,这些细胞的主要粘附蛋白(E-钙粘蛋白)在微腔(microlumen)的边缘聚集在一起。就像在页岩气水力压裂中一样,来自囊胚腔的加压液体被注入在两个粘性细胞膜之间,将它们分裂开并将它们的E-钙粘蛋白重新分布到新形成的微腔边缘的新位置上。
在经过一段时间的大量水力压裂之后,粗化阶段(coarsening phase)开始,一些气泡变大,然后较大的微腔聚集在一起,直到它们形成一个大腔,从而将胚胎细胞团转移到囊胚的一半中。
8.Science:重磅!三维打印人类心脏不再是遥远的梦
doi:10.1126/science.aav9051; doi:10.1126/science.aay0478
在一项新的研究中,来自美国卡内基梅隆大学的研究人员详细介绍了一种新技术,它允许任何人利用人体中一种称为胶原蛋白的主要结构蛋白对组织支架进行三维生物打印(3-D bioprinting)。这种首创的方法使得组织工程领域更接近于能够三维打印全尺寸的成人心脏 。相关研究结果发表在2019年8月2日的Science期刊上,论文标题为“3D bioprinting of collagen to rebuild components of the human heart”。
这种称为悬浮水凝胶自由可逆嵌入(Freeform Reversible Embedding of Suspended Hydrogels, FRESH)的技术允许这些研究人员克服与现有三维生物打印方法相关的许多挑战,并使用柔软的生物材料实现前所未有的分辨率和保真度。
人体中的每个器官,比如心脏,是由称为细胞外基质(ECM)的生物支架保持在一起的特化细胞构建而成的。这种ECM蛋白网络提供了细胞执行它们的正常功能所需的结构和生化信号。然而,在此之前,人们还不可能使用传统的生物制造方法重建这种复杂的ECM结构。
论文通讯作者、卡内基梅隆大学生物医学工程教授、材料科学与工程教授Adam Feinberg说道,“我们所展示的是我们能够利用细胞和胶原蛋白打印出心脏的多个真正发挥作用的部分,比如心脏瓣膜,或较小的能够搏动的心室。通过使用人类心脏的MRI数据,我们能够准 确地重建患者特有的解剖结构,并且利用胶原蛋白和人心脏细胞进行三维生物打印。”
9.Science:癌症无法终结?新研究带来新的见解
doi:10.1126/science.aau9923; doi:10.1126/science.aay2859
如果能从癌症中找到什么安慰的话,那就是这种毁灭性的疾病会随着患者的死亡而消亡。至少长期以来人们是这么认为的。然而,在一项新的研究中,来自英国、澳大利亚、美国、苏里南、印度、智利、巴拿马、格林纳达、肯尼亚、伯利兹、巴西、南非、墨西哥、尼加 拉瓜、尼日利亚、希腊、萨摩亚、俄罗斯、委内瑞拉、葡萄牙、乌克兰、塞内加尔、荷兰、亚美尼亚、乌拉圭、法国、意大利、厄瓜多尔、冈比亚、乌干达、哥伦比亚、奥地利、巴基斯坦、罗马尼亚、土耳其、巴拉圭和马拉维的研究人员发现了一些可传播的癌症,可从 一个宿主传播到另一个宿主。事实上,一种称为犬传染性性病瘤(canine transmissible venereal tumor, CTVT)的传染性癌症已成功地在狗身上持续存在了数千年。相关研究结果发表在2019年8月2日的Science期刊上,论文标题为“Somatic evolution and global expansion of an ancient transmissible cancer lineage”。
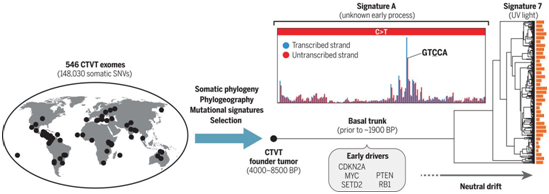
在一篇发表在同期Science期刊上的标题为“Cancer cell evolution through the ages”的评论性文章中,Carlo Maley和Darryl Shibata描述了这种性传播疾病的动态变化。这种疾病起源于一种生活在8500年前的古老动物。
有趣的是,对CTVT的中长期多代癌症进化的探索可能会对人类癌症在典型的疾病过程中如何进化提供新的线索,并且可能启发治疗癌症的新方法,这是因为它仍然是全球第二大死亡原因。
Maley说,“癌症在进化,我们控制癌症的策略需要考虑到这一点。在未来,我们希望保持对这些不断进化的肿瘤的长期控制。CTVT是非常吸引人的,这是因为它向我们展示了癌症如何在长期内进化。”
10.Science:重大进展!揭示阿尔茨海默病致病机制
doi:10.1126/science.aay0198; doi:10.1126/science.aay5188
大脑特定区域中过度活跃的神经元被认为是阿尔茨海默病的早期扰动。在一项新的研究中,来自德国慕尼黑工业大学的研究人员首次能够解释这一早期重要的神经功能障碍的原因和机制。他们发现,兴奋性神经递质谷氨酸在活跃的神经元附近持续存在过长时间。这导致这些神经元遭受病理性过度刺激,这很可能是阿尔茨海默病患者学习和记忆丧失的关键因素。相关研究结果发表在2019年8月9日的Science期刊上,论文标题为“A vicious cycle of β amyloid–dependent neuronal hyperactivation”。
神经元使用称为神经递质的化学物质进行相互沟通。作为其中最为重要的化学物质之一,谷氨酸起着激活连接在一起的神经元的作用。谷氨酸被释放在两个神经元之间的称为突触的连接位点上,并且被快速移除以允许传播下一个信号。这种移除涉及所谓的活性泵分子以及谷氨酸沿着附近的细胞膜进行被动转运。
这些研究人员发现高浓度的谷氨酸在高度活跃的神经元的突触间隙中持续存在过长时间。这是由于β-淀粉样蛋白分子的作用:它们阻止谷氨酸从突触间隙转运出来。他们使用来自患者样本的β-淀粉样蛋白分子并使用各种小鼠模型测试了这种机制,都获得了类似结果。
这些研究人员还发现这种神经递质阻断是由早期可溶性β-淀粉样蛋白而不是斑块介导的。β-淀粉样蛋白最初以单分子形式(单体)存在,然后聚集成双分子形式(二聚体)和更大的β-淀粉样蛋白链,最终形成斑块。他们发现谷氨酸阻断是由可溶性的β-淀粉样蛋白二聚体引起的。(生物谷 Bioon.com)
1.Science:重大突破!CRISPR-Cas系统新用途!开发出可编程的CRISPR反应性智能材料
doi:10.1126/science.aaw5122; doi:10.1126/science.aay4198
CRISPR-Cas系统已成为科学家们在不断增加的有机体中研究基因的首选工具,并且正被用于开发潜在地校正基因组中单个核苷酸位点上的缺陷的新型基因疗法。它也被用于正在进行的诊断方法中,用于检测患者体内的病原体和致病突变。
如今,在一项新的研究中,来自美国哈佛大学威斯生物启发工程研究所和麻省理工学院的研究人员展示了将CRISPR用作新型刺激反应性“智能(smart)”材料的控制元件。一旦被特定的天然的或用户定义的DNA刺激物激活,一种CRISPR-Cas酶就能够让多种智能材料释放出自身结合的货物,比如染料和活性酶,改变它们的结构来部署包埋的纳米颗粒和活细胞,或者调节电路从而将生物信号转化为电信号。相关研究结果发表在2019年8月23日的Science期刊上,论文标题为“Programmable CRISPR-responsive smart materials”。

图片来自Science, 2019, doi:10.1126/science.aaw5122。
论文通讯作者、哈佛大学威斯生物启发工程研究所创始核心学院成员James Collins博士说,“我们的研究表明CRISPR的力量可以在实验室之外用于控制DNA反应性材料的行为。我们开发了一系列具有不同能力的材料,这就突显了可编程的CRISPR反应性智能材料(CRISPR-responsive smart material)所支持的应用范围。这些应用包括新型治疗诊断策略、即时诊断以及对流行病爆发和环境危害进行的区域监测。”
论文共同第一作者、麻省理工学院研究生Max English说,“我们将单链靶DNA序列整合到聚合物材料中,要么作为悬垂货物的锚点,要么作为维持材料基本完整性的结构元件,并且能够通过提供Cas12a和一种作为刺激物的特定gRNA来控制不同的材料行为。”
2.Science:构建出疟原虫完整生命周期的细胞图谱---疟疾细胞图谱,极大加快疟疾研究和疗法开发
doi:10.1126/science.aaw2619; doi:10.1126/science.aay5963
在一项新的研究中,来自英国、丹麦、肯尼亚、南非、澳大利亚、瑞典和法国的研究人员构建出疟疾细胞图谱(Malaria Cell Atlas),这种图谱呈现出疟原虫在所有形态生命周期阶段的转录组学特征。这种图谱的目标是(i)了解在整个生命周期中的基因功能和使用;(ii)理解发育阶段转变背后的基因调控机制;(iii)发现疟原虫两头下注(bet-hedging)模式;(iv)提供一种参考数据集,可用于了解多种疟原虫物种在实验室中和在自然感染下的寄生虫生物学特性。相关研究结果发表在2019年8月23日的Science期刊上,论文标题为“The Malaria Cell Atlas: Single parasite transcriptomes across the complete Plasmodium life cycle”。
这些研究人员通过使用细胞分选方法分离出1787个疟原虫,并且在涵盖蚊子和哺乳动物宿主中所有生命周期阶段的10个时间点对它们的全长转录组进行了分析。
从这些数据中,他们能够了解发育的精细转录模式,并确定与疟原虫阶段、细胞策略(增殖阶段、生长阶段和有性阶段)和宿主环境相关的标志基因。对整个生命周期中的单细胞基因表达模式的比较揭示出在发育过程中有几组基因的表达模式相似。由此产生的行为相似的基因簇能够推断出仍然未被表征的大约40%基因的可能功能。
通过使用液滴测序,这些研究人员对来自三种疟原虫物种(包括两种人类疟原虫病原体)的红细胞内发育周期的另外15858个细胞进行了测序。他们在生命周期的致病阶段对这三种疟原虫物种的发育轨迹进行了比对,并建立了一种跨物种比较的方法。最后,他们开发出一种保存从天然的受感染携带者中收集的野生疟原虫的实验方案,使用scRNA-seq进行测序,并将疟疾细胞图谱作为参考,以便鉴定出野生疟原虫发育阶段并在单细胞分辨率下表征天然的混合物种感染。
3.Science:植物免疫系统新突破!揭示植物TIR结构域是一种促进细胞死亡的NAD+切割酶
doi:10.1126/science.aax1771
在一项新的研究中,一组研究人员阐明了植物免疫反应的一个关键方面。他们的发现揭示了植物抗性蛋白如何引发局部的细胞死亡,这可能导致人们在下一代作物中开发出进行抗病性改造的新策略。相关研究结果发表在2019年8月23日的Science期刊上,论文标题为“TIR domains of plant immune receptors are NAD+-cleaving enzymes that promote cell death”。论文通讯作者为科罗拉多州立大学生物学助理教授Marc Nishimura、北卡罗来纳大学教堂山分校的Jeff Dangl和华盛顿大学医学院的Jeffrey Milbrandt。

图片来自Marc Nishimura/Colorado State University。
Nishimura与其同事们一起鉴定出植物抗性蛋白TIR的一种鲜为人知的结构域(即TIR结构域)的作用机制。他们发现在植物免疫反应期间,这种TIR结构域是一种降解NAD+分子的酶,其中NAD+分子对所有生物的新陈代谢至关重要。通过切割NAD+,植物自我破坏受感染的细胞,同时不会伤害其他未被感染的细胞。
在2017年,Nishimura在华盛顿大学医学院的合作者在一种名为SARM1的蛋白中观察到一种不寻常的动物TIR结构域,它不同于动物细胞中的其他TIR信号支架。相反,它作为一种酶发挥作用。Nishimura及其同事们开始探究这种结构域是否在植物免疫系统中发挥着具有类似的功能。
在这项新的研究中,Nishimura及其同事们发现TIR结构域在植物免疫反应中的作用确实与SARM1中功能上更不寻常的这种动物TIR结构域的作用相关。他们发现植物TIR结构域本身就是一种切割NAD+的酶,而不是作为招募其他成分的结构支架起作用。但是还存在一个重要的区别。虽然SARM1中的动物TIR结构域通过消耗NAD+水平来杀死细胞,但植物TIR结构域似乎切割NAD+来产生信号分子。这种并未在动物细胞中观察到的信号分子在结构上一种与称为环状ADP-核糖(cyclic ADP-Ribose)的经典信号分子有关。他们如今正在努力了解他们观察到的这种新产物如何影响细胞死亡和抗病能力。
4.Science:打破教科书! 皮肤中发现新的疼痛器官!
doi:10.1126/science.aax6452; doi:10.1126/science.aay6144
瑞典卡罗林斯卡学院的研究人员发现了一种新的感觉器官,它可以检测到疼痛的机械损伤,比如刺痛和撞击。这项发现发表在《Science》杂志上。
疼痛造成痛苦,并给社会带来巨大的经济损失。几乎每五个人中就有一个人经历持续的疼痛,因此很有必要寻找新的止痛药物。然而,对疼痛的敏感也是生存所必需的,它具有保护功能。它能促进防止损伤组织的反射反应,比如当你感到被尖锐物体刺痛或烧伤时把手抽离。
卡罗林斯卡学院的研究人员现在在皮肤上发现了一种新的感觉器官,它对有害的环境刺激很敏感。它由神经胶质细胞组成,有多个长长的突起,共同构成皮肤内网状的器官。这个器官对刺痛和压力等痛苦的机械损伤很敏感。
这项研究描述了新的痛觉器官的特点--它是如何与皮肤中的痛觉神经组织在一起的,以及该器官的激活如何导致神经系统中的电脉冲,从而导致反射反应和疼痛体验。组成器官的细胞对机械刺激高度敏感,这就解释了它们如何参与检测疼痛的针刺和压力。在实验中,研究人员还阻断了该器官的活动,从而导致机械疼痛的感觉能力下降。
5.Science重大突破:肠道细菌竟然可以预防肥胖!
doi:10.1126/science.aat9351
犹他大学健康学院的研究人员发现,肠道中有一种特定的细菌可以防止老鼠变胖,这表明这些细菌也可以控制人类的体重。这种有益的细菌被称为梭状芽孢杆菌(Clostridia),是微生物群落的一部分--肠道内共有数万亿的细菌和其他微生物。
近日发表在《Science》杂志上的这项研究表明,健康的老鼠体内有大量梭状芽孢杆菌(一种由20到30种细菌组成的细菌),但那些免疫系统受损的老鼠随着年龄的增长会失去这些微生物。即使喂食健康的食物,老鼠也不可避免地会变胖。把这类微生物还给这些动物可以让它们保持苗条。
这项研究的结果已经指向这个方向。Petersen和他的同事发现梭状芽孢杆菌通过阻断肠道吸收脂肪的能力来防止体重增加。实验中,梭状芽孢杆菌是小鼠肠道中唯一的细菌,与完全没有微生物群的小鼠相比,梭状芽孢杆菌的小鼠更瘦,脂肪更少。他们还拥有较低水平的CD36基因,该基因控制着身体对脂肪酸的吸收。
Round说,这些发现可能会导致一种治疗方法,它比粪便移植和益生菌更有优势--目前正被广泛研究作为恢复健康微生物群的方法。基于将活菌群转移到肠道的治疗方法并不适用于所有人,因为不同的饮食和其他因素会影响哪些细菌能够存活和繁殖。
6.Science:操纵蛋白GPR139有望更安全地使用阿片类药物
doi:10.1126/science.aau2078
在一项新的研究中,来自美国斯克里普斯研究所和堪萨斯大学的研究人员发现一种蛋白有朝一日可能经操纵后使得疼痛患者更安全地使用阿片类药物。相关研究结果于2019年8月15日在线发表在Science期刊上,论文标题为“Genetic behavioral screen identifies an orphan anti-opioid system”。
阿片类药物是一类用于减轻疼痛的药物,但是它们也很容易上瘾。不幸的是,科学家们一直无法找到阿片类药物的替代品,因此有些人已开始寻找让现有药物不那么容易上瘾的方法。在这项新的研究中,这些研究人员研究了通过遗传手段改变线虫以减少阿片类药物成瘾的方法。
这项研究涉及在线虫基因中产生900多种突变,然后对每种突变进行测试以便观察它是否导致对阿片类药物敏感性的任何变化。他们报道他们在一个称为FRPR-13的基因中发现了一种似乎可以减轻症状的突变。他们接下来在哺乳动物中发现FRPR-13同源基因,这个同源基因编码一种称为GPR139的蛋白。他们发现这种蛋白对μ-阿片受体(mu-opioid receptor, MOR)信号转导产生抑制作用。他们随后将注意力转向这个基因和这种蛋白在小鼠中的作用。他们的一项测试涉及通过遗传手段改变小鼠,从而阻止GPR139编码,这接着会阻止这种蛋白的产生。他们发现,这样做往往会增强阿片类药物(吗啡)抑制神经元放电的能力--- MOR水平下降了。最终结果就是疼痛减轻了。但是,测试还表明阻止GPR139产生导致成瘾小鼠出现更少的断瘾症状。
这些研究人员指出断瘾症状的减少可能是由于蓝斑核(locus coeruleus)中的神经元放电变化,其中蓝斑核是大脑的一部分,之前的研究表明它参与处理断瘾信号。他们最后建议GPR139有朝一日可以在减少人类患者的断瘾症状方面发挥重要作用,这会让阿片类药物变得更安全。
7.Science:受控的水力压裂让哺乳动物胚胎发育成形
doi:10.1126/science.aaw7709; doi:10.1126/science.aay2860
水力压裂(hydraulic fracturing)是一种最为常见的与页岩气开采相关的过程。在一项新的研究中,来自法国索邦大学居里研究所和法兰西学院生物跨学科研究中心的研究人员作出结论:自我压裂(self-fracking)是将胚胎(来自小鼠)从径向对称的细胞聚集体切换到双侧对称的囊胚(blastocyst)的机制。相关研究结果近期发表在Science期刊上,论文标题为“Hydraulic fracturing and active coarsening position the lumen of the mouse blastocyst”。

小鼠胚胎发育,图片来自Department of Physiology, Development and Neuroscience, University of Cambridge。
在植入之前,胚胎是一组紧密的细胞,这些细胞或多或少地径向分裂,因而大体上保持球形。随后,这些细胞变成两侧对称的囊胚---由充满液体的囊胚腔(blastocoel)、最终成为胎儿的内胚细胞团和最终变成胎盘的滋养外胚层(trophectoderm)组成。水力压裂发生在这两个步骤之间的过渡阶段;它是这些细胞如何沿着第一轴将它们的排列从径向对称切换到两侧对称。
通过使用高分辨率实时成像,这些研究人员观察到在小鼠囊胚形成过程中这种对称性破裂的过程。像往常一样,受精卵(精子和卵细胞结合形成的一个细胞)经细胞分裂后产生两个细胞,然后是四个,依此类推,直到第五轮细胞分裂,这时他们观察到“处数百个气泡在细胞-细胞连接处同步出现”,每个气泡充满着加压水。在这些气泡(微腔)的形成过程中,这些细胞的主要粘附蛋白(E-钙粘蛋白)在微腔(microlumen)的边缘聚集在一起。就像在页岩气水力压裂中一样,来自囊胚腔的加压液体被注入在两个粘性细胞膜之间,将它们分裂开并将它们的E-钙粘蛋白重新分布到新形成的微腔边缘的新位置上。
在经过一段时间的大量水力压裂之后,粗化阶段(coarsening phase)开始,一些气泡变大,然后较大的微腔聚集在一起,直到它们形成一个大腔,从而将胚胎细胞团转移到囊胚的一半中。
8.Science:重磅!三维打印人类心脏不再是遥远的梦
doi:10.1126/science.aav9051; doi:10.1126/science.aay0478
在一项新的研究中,来自美国卡内基梅隆大学的研究人员详细介绍了一种新技术,它允许任何人利用人体中一种称为胶原蛋白的主要结构蛋白对组织支架进行三维生物打印(3-D bioprinting)。这种首创的方法使得组织工程领域更接近于能够三维打印全尺寸的成人心脏 。相关研究结果发表在2019年8月2日的Science期刊上,论文标题为“3D bioprinting of collagen to rebuild components of the human heart”。
这种称为悬浮水凝胶自由可逆嵌入(Freeform Reversible Embedding of Suspended Hydrogels, FRESH)的技术允许这些研究人员克服与现有三维生物打印方法相关的许多挑战,并使用柔软的生物材料实现前所未有的分辨率和保真度。
人体中的每个器官,比如心脏,是由称为细胞外基质(ECM)的生物支架保持在一起的特化细胞构建而成的。这种ECM蛋白网络提供了细胞执行它们的正常功能所需的结构和生化信号。然而,在此之前,人们还不可能使用传统的生物制造方法重建这种复杂的ECM结构。
论文通讯作者、卡内基梅隆大学生物医学工程教授、材料科学与工程教授Adam Feinberg说道,“我们所展示的是我们能够利用细胞和胶原蛋白打印出心脏的多个真正发挥作用的部分,比如心脏瓣膜,或较小的能够搏动的心室。通过使用人类心脏的MRI数据,我们能够准 确地重建患者特有的解剖结构,并且利用胶原蛋白和人心脏细胞进行三维生物打印。”
9.Science:癌症无法终结?新研究带来新的见解
doi:10.1126/science.aau9923; doi:10.1126/science.aay2859
如果能从癌症中找到什么安慰的话,那就是这种毁灭性的疾病会随着患者的死亡而消亡。至少长期以来人们是这么认为的。然而,在一项新的研究中,来自英国、澳大利亚、美国、苏里南、印度、智利、巴拿马、格林纳达、肯尼亚、伯利兹、巴西、南非、墨西哥、尼加 拉瓜、尼日利亚、希腊、萨摩亚、俄罗斯、委内瑞拉、葡萄牙、乌克兰、塞内加尔、荷兰、亚美尼亚、乌拉圭、法国、意大利、厄瓜多尔、冈比亚、乌干达、哥伦比亚、奥地利、巴基斯坦、罗马尼亚、土耳其、巴拉圭和马拉维的研究人员发现了一些可传播的癌症,可从 一个宿主传播到另一个宿主。事实上,一种称为犬传染性性病瘤(canine transmissible venereal tumor, CTVT)的传染性癌症已成功地在狗身上持续存在了数千年。相关研究结果发表在2019年8月2日的Science期刊上,论文标题为“Somatic evolution and global expansion of an ancient transmissible cancer lineage”。

图片来自Science, 2019, doi:10.1126/science.aau9923。
在一篇发表在同期Science期刊上的标题为“Cancer cell evolution through the ages”的评论性文章中,Carlo Maley和Darryl Shibata描述了这种性传播疾病的动态变化。这种疾病起源于一种生活在8500年前的古老动物。
有趣的是,对CTVT的中长期多代癌症进化的探索可能会对人类癌症在典型的疾病过程中如何进化提供新的线索,并且可能启发治疗癌症的新方法,这是因为它仍然是全球第二大死亡原因。
Maley说,“癌症在进化,我们控制癌症的策略需要考虑到这一点。在未来,我们希望保持对这些不断进化的肿瘤的长期控制。CTVT是非常吸引人的,这是因为它向我们展示了癌症如何在长期内进化。”
10.Science:重大进展!揭示阿尔茨海默病致病机制
doi:10.1126/science.aay0198; doi:10.1126/science.aay5188
大脑特定区域中过度活跃的神经元被认为是阿尔茨海默病的早期扰动。在一项新的研究中,来自德国慕尼黑工业大学的研究人员首次能够解释这一早期重要的神经功能障碍的原因和机制。他们发现,兴奋性神经递质谷氨酸在活跃的神经元附近持续存在过长时间。这导致这些神经元遭受病理性过度刺激,这很可能是阿尔茨海默病患者学习和记忆丧失的关键因素。相关研究结果发表在2019年8月9日的Science期刊上,论文标题为“A vicious cycle of β amyloid–dependent neuronal hyperactivation”。
神经元使用称为神经递质的化学物质进行相互沟通。作为其中最为重要的化学物质之一,谷氨酸起着激活连接在一起的神经元的作用。谷氨酸被释放在两个神经元之间的称为突触的连接位点上,并且被快速移除以允许传播下一个信号。这种移除涉及所谓的活性泵分子以及谷氨酸沿着附近的细胞膜进行被动转运。
这些研究人员发现高浓度的谷氨酸在高度活跃的神经元的突触间隙中持续存在过长时间。这是由于β-淀粉样蛋白分子的作用:它们阻止谷氨酸从突触间隙转运出来。他们使用来自患者样本的β-淀粉样蛋白分子并使用各种小鼠模型测试了这种机制,都获得了类似结果。
这些研究人员还发现这种神经递质阻断是由早期可溶性β-淀粉样蛋白而不是斑块介导的。β-淀粉样蛋白最初以单分子形式(单体)存在,然后聚集成双分子形式(二聚体)和更大的β-淀粉样蛋白链,最终形成斑块。他们发现谷氨酸阻断是由可溶性的β-淀粉样蛋白二聚体引起的。(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


