胰腺癌治疗路在何方?新研究或带来希望
来源:本站原创 2019-08-11 16:55
2019年8月11日讯 /生物谷BIOON /——胰腺导管腺癌(PDAC)是最常见的胰腺癌,是美国第三大常见癌症致死原因,在英国排名第五。尽管发病率存在显着差异,但PDAC导致的死亡人数超过了乳腺癌。导致这些黯淡的统计数据最重要的原因是诊断晚和治疗无效。PDAC是一种恶性肿瘤,侵袭性强,治疗困难。到目前为止,唯一的治疗方法是彻底切除肿瘤。不幸的是,因为PDAC通常是无症状的,当它被诊断出来的时候,
2019年8月11日讯 /生物谷BIOON /——胰腺导管腺癌(PDAC)是最常见的胰腺癌,是美国第三大常见癌症致死原因,在英国排名第五。尽管发病率存在显着差异,但PDAC导致的死亡人数超过了乳腺癌。导致这些黯淡的统计数据最重要的原因是诊断晚和治疗无效。
PDAC是一种恶性肿瘤,侵袭性强,治疗困难。到目前为止,唯一的治疗方法是彻底切除肿瘤。不幸的是,因为PDAC通常是无症状的,当它被诊断出来的时候,80%到90%的病人都到了手术无法治愈的地步。因此,由于PDAC的低存活率,它仍然是当今生物医学的主要挑战之一--只有5%的患者在确诊后5年仍然存活。
然而,近几十年来,许多研究已经阐明了PDAC的形成和发展的分子机制。最近的研究表明,在治疗方面取得进展是可能的。
无效的治疗方法
胰腺癌的分子机制是复杂的。这就是为什么最近个性化医疗和免疫疗法(帮助免疫系统对抗癌症)的进展未能改善胰腺癌的治疗。这主要有两个特点:
95%的肿瘤是由KRAS致癌基因突变引起的。致癌基因是一种癌基因,一旦发生突变,就能够诱导正常细胞转变为癌细胞。KRAS是一种起开关作用的基因。正常情况下,KRAS控制细胞增殖。然而,当它发生突变时,细胞开始不受控制地生长和增殖--这是癌细胞的一个特征。到目前为止,KRAS致癌基因还无法被药物靶向。
图片来源:https://cn.bing.com
PDACs被大量纤维结缔组织所包围,这些结缔组织生长在某些肿瘤的周围。就PDAC而言,这种组织形成一种屏障,阻止识别和攻击肿瘤细胞的细胞毒T淋巴细胞进入肿瘤内部并杀死肿瘤细胞。这使得免疫治疗无效。
由于这些原因,PDAC继续被用于破坏癌细胞但也能破坏健康细胞的药物治疗。可选择的药物包括1997年批准的德西他滨和一种新的紫杉醇为基础的nab -紫杉醇。即使这样的治疗是一种选择,它通常也只能延长病人几周的生命,充其量也只能有微小的改善。
然而,近年来,许多关于PDAC发生和发展的分子机制的研究已经阐明。
今天我们知道这些肿瘤大多是由KRAS致癌基因突变引起的。它们导致良性改变,导致一系列肿瘤抑制基因发生额外突变,这些基因通常修复DNA错误,减缓细胞分裂,或告诉细胞何时死亡。突变的细胞可能会生长失控,在这种情况下进展为恶性PDAC。虽然这一过程相对为人所知,但它尚未对开发新的和更有效的治疗方法产生直接影响。
寻找新的策略
目前正在研究多种策略,试图通过阻断肿瘤细胞或其周围"屏蔽"结缔组织的生长来抑制这些肿瘤的生长。在美国国家肿瘤研究中心Mariano Barbacid的实验室中,他们专注于阻断介导KRAS致癌基因启动致癌活性的信号通路。
十年前,该实验室决定使用能够复制人类PDAC自然历史的基因工程小鼠肿瘤模型,这样做是为了分析KRAS信号通路的主要成分的治疗潜力。这些研究揭示了到目前为止测试的药物具有难以忍受的毒性作用的原因,老鼠在几周内就会死亡:它们针对的是一些蛋白质,这些蛋白质对细胞的动态平衡状态(即细胞的最佳功能状态)至关重要。这被称为正常的体内平衡。
图片来源:https://cn.bing.com
这些关键的蛋白质主要是激酶,一种能够改变其他分子功能的酶。它们在调节细胞信号和协调激素反应和细胞分裂等过程中发挥着重要而复杂的作用。这些结果也许可以解释为什么目前测试的KRAS信号抑制剂在临床试验中失败。另一方面,去除其他信号激酶没有毒副作用,但也没有影响肿瘤的发展。
在参与KRAS致癌基因信号传递的15多个激酶中,只有3个表现出显着的治疗效果,而没有引起不可接受的副作用。这些是:RAF1,表皮生长因子受体(EGFR)和CDK4。
它的工作原理!(老鼠)
在最初的研究中,研究人员观察到(通过基因操作)消除这三种激酶中的表达,可以防止KRAS致癌基因引起的PDAC的发生。然而,在晚期肿瘤动物中,它的消除没有显着的治疗效果。这些结果使研究人员怀疑是否有可能在不增加毒性作用的情况下同时消除多个激酶。
正如他们最近发表在《Cancer Cell》杂志上的工作所述,在50%的小鼠中,RAF1和EGFR表达的消除导致了晚期PDACs的完全消退。研究人员目前正在研究是否可以通过消除CDK4来增加这一比例。
在对动物胰腺的分析中,研究人员不再能够通过成像技术观察肿瘤,结果显示其中两个胰腺完全没有病变。两只小鼠显示出一些异常的导管,可能是肿瘤残留的疤痕。另一组的肿瘤微团块大小仅为原肿瘤的千分之一。这些研究揭示了肿瘤细胞的存在,其中EGFR和RAF1这两个靶点的表达尚未完全消除,这是这类研究中常见的技术问题。
值得注意的是,这些结果不仅在小鼠身上观察到。抑制来自十分之九的人类PDACs细胞中这两个蛋白表达,在移植到免疫抑制小鼠体内和体外培养时,也能阻止其在体内的增殖。
现在该做什么?
虽然这些结果目前只在小鼠的一个亚群中观察到,但它们的重要性在于,这是第一次有可能通过消除药物导向的靶点来完全消除晚期PDAC肿瘤。
这些观察结果对基于抑制RAF1和EGFR的治疗方法的发展显然是重要的,但它们只是前面漫长而艰难道路上的第一步。
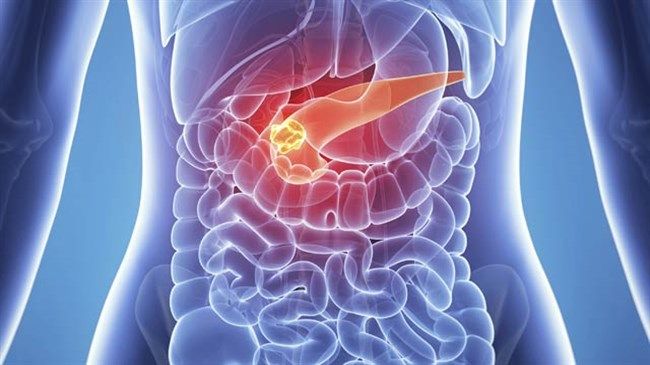
图片来源:https://cn.bing.com
首先,重要的是要确定对联合消除RAF1和EGFR有反应的PDACs与那些有耐药性的PDACs之间的差异。正如研究人员在工作中所描述的,对这两种肿瘤类型的分析表明,它们并不以相同的方式活跃--超过2000个基因表达不同。
在耐药肿瘤中确定不会增加治疗毒性的其他靶点并非易事。
为了继续对基因工程小鼠的测试,当务之急是开发特定的RAF1抑制剂,但难度并不亚于此。事实上,研究人员目前只有针对第二个目标EGFR的有效药物。原则上,有四种可能的方法:为其激酶活性生成选择性抑制剂;产生与KRAS致癌基因结合的抑制剂;为其与传递由RAF1介导的致癌信号的效应靶点的相互作用开发抑制剂;用药物降解RAF1蛋白。
鉴于制药业在设计这种分子类型方面的经验,设计RAF1激酶活性抑制剂似乎是最实惠的选择。
问题在于,同样的家族还有另外两种激酶,ARAF和BRAF,它们的催化中心(酶的"活性核心")几乎是相同的。RAF1激酶抑制剂也针对这些引起附带损害的其他激酶。到目前为止,这些药物已经造成了很高的毒性,临床试验不得不停止。
继续开发能够阻断PDAC患者RAF1活性的有效分子并不容易。这肯定比我们希望的要花更多的时间,但至少已经勾勒出一幅路线图,向我们展示了如何继续前进。(生物谷Bioon.com)
参考资料:
【1】lMaría TeresaBlasco et al. Complete Regression of Advanced Pancreatic Ductal Adenocarcinomas upon Combined Inhibition of EGFR and C-RAF. Cancer Cell. DOI:https://doi.org/10.1016/j.ccell.2019.03.002
【3】Prashanth Rawla et al. Epidemiology of Pancreatic Cancer: Global Trends, Etiology and Risk Factors. World J Oncol. 2019 Feb; 10(1): 10-27. doi: 10.14740/wjon1166
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->