罕见病新药!Arrowhead公司高胆固醇血症RNAi疗法ARO-AGN3获美国FDA授予孤儿药资格
来源:本站原创 2019-07-17 10:21
2019年07月17日/生物谷BIOON/--Arrowhead是一家临床阶段的RNAi治疗公司。近日,该公司宣布美国食品和药物管理局(FDA)已授予ARO-AGN3治疗纯合子家族性高胆固醇血症(HoFH)的孤儿药资格(ODD)。孤儿药是指用于预防、治疗、诊断罕见病的药品,而罕见病是一类发病率极低的疾病的总称,又称“孤儿病”。在美国,罕见病是指患病人群少于20万的疾病类型,罕见病药物研发方面的激励

2019年07月17日/生物谷BIOON/--Arrowhead是一家临床阶段的RNAi治疗公司。近日,该公司宣布美国食品和药物管理局(FDA)已授予ARO-AGN3治疗纯合子家族性高胆固醇血症(HoFH)的孤儿药资格(ODD)。
孤儿药是指用于预防、治疗、诊断罕见病的药品,而罕见病是一类发病率极低的疾病的总称,又称“孤儿病”。在美国,罕见病是指患病人群少于20万的疾病类型,罕见病药物研发方面的激励措施包括各种临床开发激励措施,如临床试验费用相关的税收抵免、FDA用户费减免、临床试验设计中FDA的协助,以及药物获批上市后为期7年的市场独占期。
HoFH是一种罕见的遗传性脂蛋白代谢紊乱,这是一种危及生命的疾病,其特征是低密度脂蛋白胆固醇(LDL-C)显著升高,导致早发性的心血管疾病。如果不进行适当的治疗,动脉壁中的胆固醇积累会导致早期动脉粥样硬化和心血管疾病,即使是在儿童时期也是如此。
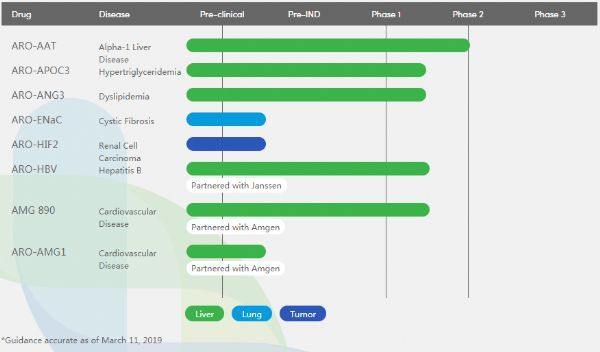
ARO-AGN3是一种皮下注射的RNA干扰(RNAi)药物,靶向血管生成素样蛋白3(ANGPTL3),这是一种由肝脏合成的脂蛋白脂酶和内皮脂酶抑制剂。抑制ANGPTL3已被证实可降低血清LDL、血清和肝脏甘油三酯,作为一个新颖的心血管疾病靶点已经获遗传学验证。目前,ARO-AGN3正开发用于治疗血脂异常(如HoFH)和代谢性疾病。
今年1月,ARO-ANG3在首个人体研究(AROANG1001,NCT03747224)启动了患者治疗。该研究是一项单剂量和多剂量I期研究,旨在评估ARO-ANG3在成人健康志愿者和血脂异常患者中的安全性、耐受性、药代动力学和药效学效应,研究计划招募70例受试者。
Arrowhead公司致力于通过抑制引起顽固性疾病的基因来开发治疗这些疾病药物。利用广泛的RNA化学和有效的递送方式,该公司旨在触发RNA干扰(RNAi)机制,诱导目标基因的快速、深度、持久的敲除。RNA干扰(即RNAi)是细胞中存在的一种机制,抑制特定基因的表达,从而影响特定蛋白质的产生。Arrowhead公司的RNAi疗法利用了基因沉默的天然途径。目前,该公司已有多个实验性RNAi疗法进入临床开发。
今年4月,该公司另一款RNAi药物ARO-AAT获FDA批准推进一项适应性II/III期研究,该研究有可能作为ARO-AAT的关键注册研究。ARO-AAT是该公司第二代皮下给药的RNAi疗法,目前正被开发用于治疗与α-1抗胰蛋白酶缺乏(AATD)相关的肝病,这是一种罕见的遗传性肝病,严重损害受影响个体的肝脏和肺脏。ARO-AAT旨在抑制突变的α-1抗胰蛋白酶(Z-AAT)蛋白在肝脏的产生,这是AATD患者进行性肝病的原因。减少炎症性Z-AAT蛋白的产生有望阻止肝病的进展,并可能使其再生和修复。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->