多发性硬化症新药!新基新型口服亚型选择性S1P受体调节剂ozanimod在美欧进入审查
来源:本站原创 2019-06-10 09:11
2019年06月10日讯 /生物谷BIOON/ --新基(Celgene)近日宣布,美国FDA已受理ozanimod治疗复发型多发性硬化症(RMS)的新药申请(NDA),欧洲药品管理局(EMA)也已受理ozanimod治疗复发缓解型多发性硬化症(RRMS)的上市许可申请(MAA)。ozanimod是一种口服1-磷酸鞘氨醇(S1P)受体调节剂,能够以高亲和力选择性结合S1P亚型1(S1P1)和亚型5

2019年06月10日讯 /生物谷BIOON/ --新基(Celgene)近日宣布,美国FDA已受理ozanimod治疗复发型多发性硬化症(RMS)的新药申请(NDA),欧洲药品管理局(EMA)也已受理ozanimod治疗复发缓解型多发性硬化症(RRMS)的上市许可申请(MAA)。
ozanimod是一种口服1-磷酸鞘氨醇(S1P)受体调节剂,能够以高亲和力选择性结合S1P亚型1(S1P1)和亚型5(S1P5)。根据处方药用户收费法(PDUFA),FDA将在2020年3月25日作出审查决定。EMA预计将在2020年上半年作出审查决定。
ozanimod是新基在2015年豪掷73亿美元收购Receptos公司的核心资产。在美国监管方面,2018年早些时候ozanimod曾遭到FDA拒绝,理由是非临床和临床药理学证据不足以允许通过审查。
此次NDA和MAA,是基于2项多中心、随机、双盲、双模拟、阳性药物对照III期临床研究SUNBEAM和RADIANCE Part B的疗效和安全性数据。新基首席医疗官Jay Backstrom表示,“FDA和EMA受理我们的申请,是我们努力将ozanimod带给患者方面的关键一步。我们相信,ozanimod有潜力成为复发型MS早期治疗的一个重要治疗选择,并成为同类最佳的S1P受体调节剂。”
值得一提的是,今年3月底,诺华口服药物Mayzent(siponimod)获FDA批准,用于RMS成人患者的治疗,包括活动性继发进展型多发性硬化症(SPMS)、复发缓解型多发性硬化症(RRMS)、临床孤立综合征(CIS)。Mayzent是过去15年来首个也是唯一一个专门批准用于活动性SPMS患者的治疗药物,其活性药物成分为siponimod,这是一种新一代、选择性1-磷酸鞘氨醇(S1P)受体调节剂,能选择性地与S1P1和S1P5受体结合,作用机理与新基ozanimod相同。
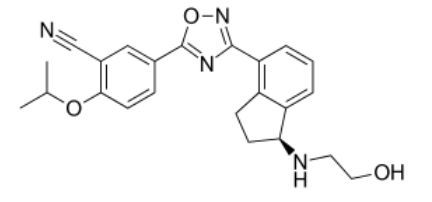
ozanimod分子结构式(图片来源:Wikipedia)
ozanimod是一种新型、口服、选择性1-磷酸鞘氨醇(S1P)受体1(S1PR1)与受体5(S1PR5)调节剂,目前正开发用于多种免疫炎症适应症,包括RMS、溃疡性结肠炎(UC)、克罗恩病(CD)。ozanimod选择性结合S1PR1被认为能够抑制一个特定亚组的活化淋巴细胞迁移到炎症区域,减少可导致抗炎活性的循环T淋巴细胞与B淋巴细胞的水平,从而缓解免疫系统对神经髓鞘进行攻击。值得一提的是,由于ozanimod的特殊作用机理,患者的免疫监视机能得以维持。而ozanimod与S1PR5的结合则能激活中枢神经系统内的特殊细胞,促进髓鞘再生,并预防突触出现缺陷,最终可预防神经损伤。在“减少损伤+加强修复”这2种机制的共同作用下,ozanimod 有潜力改善多种免疫疾病的症状。
多发性硬化症(MS)是一种慢性炎症性脱髓鞘中枢神经系统疾病,影响全球约230万人。该病是由于人体免疫系统异常攻击神经外部的绝缘层和支撑结构——髓鞘,引起炎症及相关损伤。这种损伤会破坏大脑与身体其他部位之间的信息交流,最终,神经系统本身状况会恶化,目前这一过程是不可逆转的。患者症状和体征会有很大的不同,这取决于损伤的数量和受影响的神经。部分患者可能会失去独立行走的能力,而另一些患者则可能经历长时间的缓解期,不出现新的症状。多发性硬化症的平均发病年龄一般在20至40岁,是青壮年群体中非外伤致残的主要原因。
RMS是最常见类型的MS,其特征为病情反复发作,其次是存在明显的部分或完全缓解期,在这期间症状得到部分或完全改善并且无明显的疾病进展。RMS约占初诊患者总体比例的85%,而进展型MS约占10-15%。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


