胚胎干细胞研究新近进展(第3期)
来源:本站原创 2019-04-28 21:24
2019年4月28日讯/生物谷BIOON/---胚胎干细胞,是一种具有持久更新能力的细胞,它能够或发育成几乎所有人类的各种组织或器官,故其在医学上具有非常重要的研究价值与应用前景。 人胚胎干细胞是在人胚胎发育早期——囊胚(受精后约5—7天)中未分化的细胞。囊胚含有约140个细胞,外表是一层扁平细胞,称滋养层,可发育成胚胎的支持组织如胎盘等。中心的腔称囊胚腔,腔内一侧的细胞群,称内细胞群,这些未分化
2019年4月28日讯/生物谷BIOON/---胚胎干细胞,是一种具有持久更新能力的细胞,它能够或发育成几乎所有人类的各种组织或器官,故其在医学上具有非常重要的研究价值与应用前景。 人胚胎干细胞是在人胚胎发育早期——囊胚(受精后约5—7天)中未分化的细胞。囊胚含有约140个细胞,外表是一层扁平细胞,称滋养层,可发育成胚胎的支持组织如胎盘等。中心的腔称囊胚腔,腔内一侧的细胞群,称内细胞群,这些未分化的细胞可进一步分裂、分化,发育成个体。内细胞群在形成内、中、外三个胚层时开始分化。每个胚层将分别分化形成人体的各种组织和器官,如外胚层将分化为皮肤、眼睛和神经系统等,中胚层将形成骨骼、血液和肌肉等组织,内胚层将分化为肝、肺和肠等。由于内细胞群可以发育成完整的个体,因而这些细胞被认为具有全能性。当内细胞群在培养皿中培养时,我们称之为胚胎干细胞。
通常人胚胎干细胞的来源有四种:选择性流产的人类胚胎组织;治疗不孕症夫妇不需要的由体外受精产生的人类胚胎;由捐献者专门为研究所捐献的配子由体外受精产生的人类胚胎;由体细胞核移植技术将人体细胞核移植入人或动物的卵泡内产生人类胚胎或嵌合体胚胎。
小编针对近年来胚胎干细胞研究取得的最新进展进行一番盘点,以飨读者。
1.Sci Adv:科学家鉴别出营养有效性和胚胎生长发育之间的分子关联
doi:10.1126/sciadv.aav2448
近日,一项刊登在国际杂志Science Advances上的研究报告中,来自巴塞罗那基因组调控中心的研究人员通过研究鉴别出了一种调节干细胞分裂速度的分子机制,相关研究发现有望帮助阐明人类不育发生的机制并开发新型的不育疗法。文章中,研究者描述了AHCY蛋白质的一种未知的功能,AHCY能够直接调节胚胎干细胞中基因的激活,鉴于此,研究人员将分子、细胞和计算机工具进行结合描述了与胚胎干细胞基因组相结合的特殊蛋白质,研究者Aranda说道,我们能够设法获得胚胎干细胞中蛋白质组的快照信息,这就能为我们提供一些意外的发现,比如我们就发现,包括AHCY在内的特殊代谢酶类的存在能够直接与基因调节相关联。
本文研究结果不仅表明,AHCY能作为一种激活调节子外,还阐明了胚胎发育期间营养物质代谢、基因组调节和多能干细胞分裂速度之间的关联;营养物质的存在对于胚胎的发育生长至关重要,这项研究中研究人员在分子水平下阐明了营养有效性和胚胎干细胞分裂速度之间的关联是如何被建立的。
同时研究者还表示,本文研究对于科学家们进行人类不育研究也具有重要的意义,研究人员前期的研究结果表明,AHCY蛋白能在人类机体中扮演一种不可替代的角色;如今研究人员想通过研究来调查人类机体中AHCY和胚胎发育期间缺陷之间的可能性关联,同时这也将能够为研究人员提供相关工具进行分子诊断并预测人类可能出现的生育问题。
2.Stem Cell Reports:尼古丁会影响胚胎的健康发育
doi:10.1016/j.stemcr.2019.01.022
研究人员2月28日在《Stem Cell Reports》杂志上报道,尼古丁在个体细胞水平上对人类胚胎发育产生广泛的不利影响。人胚胎干细胞(hESC)衍生的胚状体的单细胞RNA测序显示,3周的尼古丁暴露会破坏细胞间的通讯,降低细胞存活率,并改变调节心肌等关键功能的基因的表达。
作者说,这种干细胞模型提供了尼古丁对发育中胎儿个体器官和细胞影响的新见解,可用于优化药物和环境毒性筛查。
大量研究已经阐明了尼古丁在动物中的负面影响,主要是在啮齿动物模型中。动物研究表明,怀孕期间尼古丁暴露对胎儿发育有不利影响。但由于种间差异,这项研究是否可以转化为人类仍然值得怀疑。虽然其他研究通过大量RNA测序分析检测了使用人体细胞的尼古丁毒性,但这些常规研究不允许研究人员研究单细胞水平的影响。因此,尼古丁对人类胚胎发育的影响和潜在的分子机制仍然知之甚少。
为了解决这些局限性,Wu和他的合作者使用单细胞RNA测序来分析21天尼古丁暴露对由hESC衍生的胚状体产生的总共12,500个细胞的转录组的影响,所述胚胎体是不同的3-D聚集体。多能细胞的类型,产生大脑,心脏,肝脏,血管,肌肉和其他器官。他们发现细胞存活率下降,表明尼古丁早在植入前阶段就会影响胚胎发育。尼古丁暴露也降低了胚状体的大小,增加了被称为活性氧物质的破坏性分子的水平,并导致胚状体的异常形成和分化。此外,尼古丁暴露改变了从hESC分化的广泛的祖细胞中的细胞周期,并导致细胞间通讯失调,这是另一种尚未得到充分研究的副作用。他们还发现,尼古丁暴露导致金属毒性和破坏线粒体功能,脑畸形和智力残疾,肌肉发育和疾病,肺病以及影响心肌细胞收缩性的Ca2 +相关心律失常的基因表达改变。
3.Cell Stem Cell:研究人员开发出大脑类器官用于研究认知障碍!
doi:10.1016/j.stem.2018.12.015
来自耶鲁大学的研究人员近日在实验室培养皿中模拟了两种大脑结构以及它们之间的相互作用,为揭示神经精神疾病的起因带来了曙光。
耶鲁大学遗传学副教授In-Hyun Park及其团队创造了大脑中丘脑的类器官,丘脑是整合感觉信息并将之传递给大脑不同部位的重要集成器。研究人员通过干细胞创造了类器官以模拟大脑的不同区域并评估它们的功能。研究人员对丘脑感兴趣是因为有几种精神疾病和丘脑有关系。

研究人员随后将这种丘脑类器官与大脑另一个部位——额皮质的类器官融合在一起,额皮质具有更高级的认知功能。“现在我们正在尝试使用这种类丘脑去研究癫痫、自闭症、精神分裂症甚至是抑郁症。许多患这些疾病的人的额皮质和丘脑之间的联系存在缺陷,同时丘脑的微观结构也发生了改变。”
通过利用直接从病人身上提取的细胞创造类器官,研究人员可能发现每种疾病背后特殊的大脑结构的变化,可能有助于开发出个性化治疗方法。相关研究结果于近日发表在《Cell Stem Cell》上。
4.Stem Cell Rep:重磅!科学家在小鼠体内成功制造出可供移植的功能性B细胞
doi:10.1016/j.stemcr.2019.01.006
近日,一项刊登在国际杂志Stem Cell Reports上的研究报告中,来自McGovern医学院的科学家们通过研究发现,由小鼠胚胎干细胞衍生的功能性B-1细胞在移植到小鼠机体后能长期植入并分泌天然抗体,研究者非常感兴趣研究多能干细胞产生的B-1细胞,因为其能作为一种新型疗法来治疗多种免疫性障碍。
骨髓移植可能无法重建一些被称为B-1的免疫细胞(其能产生IgM抗体抵御机体新型感染),除了接受干细胞移植的患者外,IgM的缺失或许也会在多种疾病患者中发生,其会增加患者发生致死性感染的风险,这些疾病包括某些癌症、免疫性疾病、过敏性疾病和胃肠道疾病等。这项研究中,研究者实现了在不通过基因修饰的前提下利用小鼠胚胎干细胞制造功能性、可供移植的B-1细胞的目的,因此他们就能利用高质量的细胞系来支持B细胞发育,当移植到受体小鼠机体后,干细胞衍生的B细胞祖细胞就能发育成为B-1细胞,其能维持6个月以上时间,同时还能分泌天然的IgM抗体。
研究者Yoshimoto说道,在体外利用小鼠胚胎干细胞制造功能性的B-1祖细胞能够帮助开发新型细胞疗法从而提供天然的IgM以及骨髓移植无法提供的B-1细胞。未来研究人员希望能够深入研究尝试利用人类诱导多能干细胞产生B细胞,这或许能用作新型细胞疗法来治疗免疫性障碍的患者,而且相关研究结果未来有望应用于人类临床研究中。
5.Cell Stem Cell:重大突破!首次诱导多能干细胞产生杀死肿瘤细胞的成熟T细胞
doi:10.1016/j.stem.2018.12.011
在一项新的研究中,来自美国加州大学旧金山分校的研究人员首次证实他们开发出的一种技术诱导多能干细胞---它们能够产生体内的每种细胞类型,并且可在实验室里无限制地生长---产生能够杀死肿瘤细胞的成熟T细胞。这种技术使用一种称为人工胸腺类器官(thymic organoids)的三维结构。这种人工胸腺类器官通过模拟胸腺环境发挥作用。在胸腺中,T细胞是由造血干细胞产生的。相关研究结果于2019年1月17日在线发表在Cell Stem Cell期刊上,论文标题为“Organoid-Induced Differentiation of Conventional T Cells from Human Pluripotent Stem Cells”。论文通讯作者为加州大学旧金山分校的Gay Crooks博士。
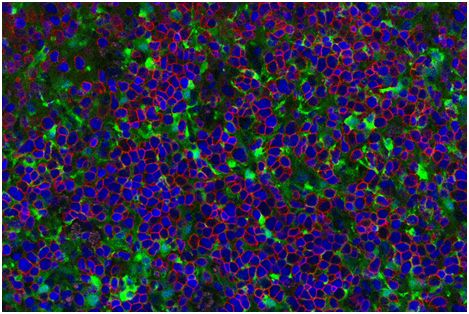
T细胞是抵抗感染的免疫系统细胞,但也有消除癌细胞的潜力。通过使用加州大学旧金山分校开发出的这种技术让自我更新的多能干细胞产生T细胞的能力可能导致人们开发出新的癌症免疫疗法,并可能促进人们进一步研究针对HIV等病毒感染和自身免疫疾病的T细胞疗法。这种技术最有希望的一个方面是它可以与基因编辑方法相结合,以便创造出几乎无限制的T细胞供应用于大量患者体内而无需使用患者自己的T细胞。
这项新的研究证实人工胸腺类器官能够让目前用于研究的两种多能性干细胞高效地产生成熟的T细胞。这两种多能干细胞是胚胎干细胞,来自于捐赠的胚胎;诱导性多能干细胞,是通过让成体皮肤细胞或血细胞经过重编程后返回到一种胚胎样状态而产生的。
这些研究人员还证实他们能够对多能干细胞进行基因改造,让它们表达一种靶向癌症的T细胞受体,并且利用人工胸腺类器官,让它们产生能够在小鼠体内靶向和杀死肿瘤细胞的T细胞。
6.Nat Commun:如何维持胚胎干细胞的无限潜能?
doi:10.1038/s41467-018-07528-9
近日,一项刊登在国际杂志Nature Communications上的研究报告中,来自索尔克研究所的科学家们通过研究开发了一种新型蛋白复合体,其能抑制干细胞的发展,从而使其能够维持无限的潜能;这种名为GBAF的复合体或有望作为后期科学家们开发新型再生医学疗法的潜在靶点。
研究者Diana Hargreaves教授表示,这项研究中,我们始于对胚胎干细胞多能性的探索,这种多能性能够促进胚胎干细胞转化成为机体中任何一种类型的细胞,阐明控制干细胞多潜能性的多种基因网络非常重要,因此能够找到一种在这一调节过程中扮演关键角色的未知蛋白,对于研究者而言也是非常有意义的。机体中的每一个细胞都有着相同的一套DNA元件,其包含有制造每一种可能性细胞类型的指令;大型的蛋白复合体(染色质重塑器)能够激活或沉默基因的表达,指导胚胎干细胞进入到一种特殊的路径中,就好比一群计划装修房子的承包商们,这些蛋复合体也包含有多重亚单位,不同亚单位的组合就能够改变DNA的物理形状,并且决定哪些基因能够指挥干细胞分化成为肺部细胞或大脑细胞。
文章中,研究人员想通过研究深入理解这些亚单位的聚集方式以及特殊的亚单位如何指挥蛋白复合体的功能,因此研究人员转向对一种名为BRD9的蛋白进行研究,该蛋白与BAF染色质重塑器家族有关,他们推测该蛋白或是其中的一种亚单位;随后研究者将BRD9化学抑制剂应用于胚胎干细胞中,并进行了一系列实验来全面分析与BAF复合体活性改变相关的细胞多潜能性。
研究者发现,BRD9能扮演胚胎干细胞发育制动器的角色,当BRD9开始发挥作用时,细胞就会维持多潜能性,而当BRD9的活性被抑制时,细胞就会开始发育的下一个阶段,随后研究者鉴别出了哪种BAF复合体能在细胞中发挥作用,结果表明,BRD9或许是一种未知BAF复合体的一部分。
7.Int J Mol Sci:转基因小鼠胚胎干细胞中Hes1和Msx1的激活增加成神经嵴衍生物的表达
doi:10.3390/ijms19124025
神经嵴(NC)包括多能细胞群,其产生外周神经元,软骨和平滑肌细胞,以及其他表型。当在经历NC分化的小鼠胚胎干细胞(mESC)中表达时,Hes1和Msx1的作用尚未可知。
在这项工作中,我们生成稳定的mESCs转染编码嵌合蛋白的构建体,其中糖皮质激素受体(GR)的配体结合域,通过加入地塞米松转移到细胞核,与Hes1(HGR)或Msx1(MGR)融合,以及双转基因细胞(HGR + MGR)。这些品系继续表达多能性标志物。在NC分化时,所有品系显示出明显的Sox2表达降低和Sox9,Snai1和Msx1的表达上调,表明NC定型。加入地塞米松以诱导嵌合蛋白的核转位。我们发现胶原IIa转录物在MGR细胞中增加,而HGR + MGR的共激活导致平滑肌肌动蛋白(α-Sma)转录物的显著增加。免疫染色显示HGR + MGR细胞中的活化诱导了更高比例的β-TUBULIN III +,α-SMA +和COL2A1 +细胞。
总之,这些发现表明单独或与HES-1组合的MSX-1的核转位产生软骨细胞样细胞,并且同时激活HES-1和MSX-1增加平滑肌和神经元细胞的产生。
8.Blood:通过抑制PAPD5调节TERC的转录后修饰可恢复角化不良患者的终末造血
doi:10.1182/blood-2018-11-885368
TERC(端粒酶RNA的组成成分)水平降低可导致携带TERC、PARN、NOP10、NHP2、NAF1或DKC1突变的患者发生角化障碍(DC)。抑制非经典poly(A)聚合酶PAPD5或外泌体RNA降解复合物,可部分恢复DKC1突变细胞的TERC水平,但仍不明确TERC的转录后加工的调控是否可改善角化障碍患者的造血输出。
Wilson Chun Fok等人采用一种携带常见角化不良蛋白突变(DKC1_A353V,该突变可导致端粒酶维持功能缺陷和终末造血潜能降低)的人胚胎干细胞(hESCs),来研究EXOSC3活性降低或PAPD5介导的寡腺苷化沉默对DC患者造血祖细胞功能的影响。
DKC1突变型hESCs的EXOSC3或PAPD5水平降低可功能性改善TERC水平和端粒酶活性,并伴随端粒延长和DNA损伤信号的降低。沉默PAPD5,可明显恢复DKC1突变细胞的终末造血潜能,但沉默EXOSC3无此效果。此外,研究人员还发现在分化的CD34+细胞中,PAPD5的抑制作用是持续的,伴随成熟的、功能性的TERC形成增多,提示上调PAPD5可能是逆转DC患者造血功能障碍的一种潜在策略。
9.Nat Commun:蜂王浆蛋白Royalactin能维持干细胞多能性
doi:10.1038/s41467-018-06256-4
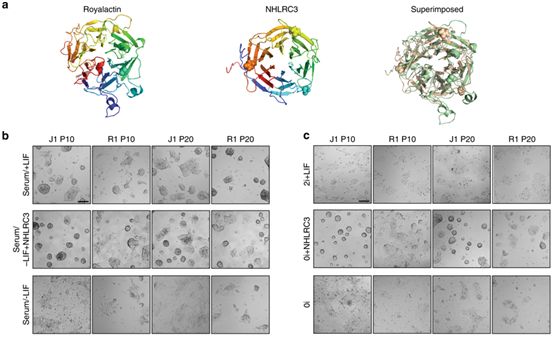
蜂王浆是蜜蜂Apis mellifera的蜂后制造者,对哺乳动物的长寿、生育和再生具有跨物种效应。尽管有这些知识,人们对蜂王浆或它的组分如何发挥其无数的作用仍然是知之甚少。在一项新的研究中,以小鼠胚胎干细胞(ESC)为平台,美国斯坦福大学的研究人员报道,蜂王浆通过它的主要蛋白组分Royalactin激活一种基态的多能性基因网络来维持这些小鼠胚胎干细胞的多能性。他们进一步鉴定出作为Royalactin的一种哺乳动物结构类似物,Regina也在小鼠胚胎干细胞中诱导出一种幼稚样状态(naive-like state)。这揭示出干细胞自我更新的一个重要的先天性程序。这些发现对于理解跨物种的干细胞命运的分子调节具有广泛的意义。
10.Sci Rep:GRG5参与胚胎和神经干细胞的转化
doi:10.1038/s41598-018-31696-9
格劳乔相关基因5(GRG5)是一种多功能蛋白,其与胚胎晚期和出生后小鼠发育有关。在这里,我们通过分析GRG5在干细胞转化决定中的功能来描述GRG5在早期发育阶段中以前未知的作用。
通过功能损失和功能获得方法,我们证明GRG5的消融使胚胎干细胞(ESC)多能状态失调,而其过表达导致自我更新能力增强和癌细胞样特性获得。由过量表达GRG5的胚胎干细胞产生的畸胎瘤的恶性特征揭示了其致癌基因潜力。此外,转录组学分析和细胞分化方法强调GRG5是抑制中内胚层相关基因的多方面信号调节因子。当ESC没有多能性时,GRG5通过Wnt和BMP信号通路抑制促进神经外胚层规范。此外,GRG5通过维持Notch/Hes和Stat3信号通路的活性来促进成纤维细胞的神经元重编程并维持神经干细胞(NSCs)的自我更新。 总之,我们的研究结果表明GRG5在干细胞生物学中具有多效作用,发挥着干细胞因子和神经转化的作用。(生物谷 Bioon.com)
通常人胚胎干细胞的来源有四种:选择性流产的人类胚胎组织;治疗不孕症夫妇不需要的由体外受精产生的人类胚胎;由捐献者专门为研究所捐献的配子由体外受精产生的人类胚胎;由体细胞核移植技术将人体细胞核移植入人或动物的卵泡内产生人类胚胎或嵌合体胚胎。
小编针对近年来胚胎干细胞研究取得的最新进展进行一番盘点,以飨读者。
1.Sci Adv:科学家鉴别出营养有效性和胚胎生长发育之间的分子关联
doi:10.1126/sciadv.aav2448
近日,一项刊登在国际杂志Science Advances上的研究报告中,来自巴塞罗那基因组调控中心的研究人员通过研究鉴别出了一种调节干细胞分裂速度的分子机制,相关研究发现有望帮助阐明人类不育发生的机制并开发新型的不育疗法。文章中,研究者描述了AHCY蛋白质的一种未知的功能,AHCY能够直接调节胚胎干细胞中基因的激活,鉴于此,研究人员将分子、细胞和计算机工具进行结合描述了与胚胎干细胞基因组相结合的特殊蛋白质,研究者Aranda说道,我们能够设法获得胚胎干细胞中蛋白质组的快照信息,这就能为我们提供一些意外的发现,比如我们就发现,包括AHCY在内的特殊代谢酶类的存在能够直接与基因调节相关联。
图片来源:CRG 2019。
本文研究结果不仅表明,AHCY能作为一种激活调节子外,还阐明了胚胎发育期间营养物质代谢、基因组调节和多能干细胞分裂速度之间的关联;营养物质的存在对于胚胎的发育生长至关重要,这项研究中研究人员在分子水平下阐明了营养有效性和胚胎干细胞分裂速度之间的关联是如何被建立的。
同时研究者还表示,本文研究对于科学家们进行人类不育研究也具有重要的意义,研究人员前期的研究结果表明,AHCY蛋白能在人类机体中扮演一种不可替代的角色;如今研究人员想通过研究来调查人类机体中AHCY和胚胎发育期间缺陷之间的可能性关联,同时这也将能够为研究人员提供相关工具进行分子诊断并预测人类可能出现的生育问题。
2.Stem Cell Reports:尼古丁会影响胚胎的健康发育
doi:10.1016/j.stemcr.2019.01.022
研究人员2月28日在《Stem Cell Reports》杂志上报道,尼古丁在个体细胞水平上对人类胚胎发育产生广泛的不利影响。人胚胎干细胞(hESC)衍生的胚状体的单细胞RNA测序显示,3周的尼古丁暴露会破坏细胞间的通讯,降低细胞存活率,并改变调节心肌等关键功能的基因的表达。
作者说,这种干细胞模型提供了尼古丁对发育中胎儿个体器官和细胞影响的新见解,可用于优化药物和环境毒性筛查。
大量研究已经阐明了尼古丁在动物中的负面影响,主要是在啮齿动物模型中。动物研究表明,怀孕期间尼古丁暴露对胎儿发育有不利影响。但由于种间差异,这项研究是否可以转化为人类仍然值得怀疑。虽然其他研究通过大量RNA测序分析检测了使用人体细胞的尼古丁毒性,但这些常规研究不允许研究人员研究单细胞水平的影响。因此,尼古丁对人类胚胎发育的影响和潜在的分子机制仍然知之甚少。
为了解决这些局限性,Wu和他的合作者使用单细胞RNA测序来分析21天尼古丁暴露对由hESC衍生的胚状体产生的总共12,500个细胞的转录组的影响,所述胚胎体是不同的3-D聚集体。多能细胞的类型,产生大脑,心脏,肝脏,血管,肌肉和其他器官。他们发现细胞存活率下降,表明尼古丁早在植入前阶段就会影响胚胎发育。尼古丁暴露也降低了胚状体的大小,增加了被称为活性氧物质的破坏性分子的水平,并导致胚状体的异常形成和分化。此外,尼古丁暴露改变了从hESC分化的广泛的祖细胞中的细胞周期,并导致细胞间通讯失调,这是另一种尚未得到充分研究的副作用。他们还发现,尼古丁暴露导致金属毒性和破坏线粒体功能,脑畸形和智力残疾,肌肉发育和疾病,肺病以及影响心肌细胞收缩性的Ca2 +相关心律失常的基因表达改变。
3.Cell Stem Cell:研究人员开发出大脑类器官用于研究认知障碍!
doi:10.1016/j.stem.2018.12.015
来自耶鲁大学的研究人员近日在实验室培养皿中模拟了两种大脑结构以及它们之间的相互作用,为揭示神经精神疾病的起因带来了曙光。
耶鲁大学遗传学副教授In-Hyun Park及其团队创造了大脑中丘脑的类器官,丘脑是整合感觉信息并将之传递给大脑不同部位的重要集成器。研究人员通过干细胞创造了类器官以模拟大脑的不同区域并评估它们的功能。研究人员对丘脑感兴趣是因为有几种精神疾病和丘脑有关系。

图片来源:Cell Stem Cell
研究人员随后将这种丘脑类器官与大脑另一个部位——额皮质的类器官融合在一起,额皮质具有更高级的认知功能。“现在我们正在尝试使用这种类丘脑去研究癫痫、自闭症、精神分裂症甚至是抑郁症。许多患这些疾病的人的额皮质和丘脑之间的联系存在缺陷,同时丘脑的微观结构也发生了改变。”
通过利用直接从病人身上提取的细胞创造类器官,研究人员可能发现每种疾病背后特殊的大脑结构的变化,可能有助于开发出个性化治疗方法。相关研究结果于近日发表在《Cell Stem Cell》上。
4.Stem Cell Rep:重磅!科学家在小鼠体内成功制造出可供移植的功能性B细胞
doi:10.1016/j.stemcr.2019.01.006
近日,一项刊登在国际杂志Stem Cell Reports上的研究报告中,来自McGovern医学院的科学家们通过研究发现,由小鼠胚胎干细胞衍生的功能性B-1细胞在移植到小鼠机体后能长期植入并分泌天然抗体,研究者非常感兴趣研究多能干细胞产生的B-1细胞,因为其能作为一种新型疗法来治疗多种免疫性障碍。
骨髓移植可能无法重建一些被称为B-1的免疫细胞(其能产生IgM抗体抵御机体新型感染),除了接受干细胞移植的患者外,IgM的缺失或许也会在多种疾病患者中发生,其会增加患者发生致死性感染的风险,这些疾病包括某些癌症、免疫性疾病、过敏性疾病和胃肠道疾病等。这项研究中,研究者实现了在不通过基因修饰的前提下利用小鼠胚胎干细胞制造功能性、可供移植的B-1细胞的目的,因此他们就能利用高质量的细胞系来支持B细胞发育,当移植到受体小鼠机体后,干细胞衍生的B细胞祖细胞就能发育成为B-1细胞,其能维持6个月以上时间,同时还能分泌天然的IgM抗体。
研究者Yoshimoto说道,在体外利用小鼠胚胎干细胞制造功能性的B-1祖细胞能够帮助开发新型细胞疗法从而提供天然的IgM以及骨髓移植无法提供的B-1细胞。未来研究人员希望能够深入研究尝试利用人类诱导多能干细胞产生B细胞,这或许能用作新型细胞疗法来治疗免疫性障碍的患者,而且相关研究结果未来有望应用于人类临床研究中。
5.Cell Stem Cell:重大突破!首次诱导多能干细胞产生杀死肿瘤细胞的成熟T细胞
doi:10.1016/j.stem.2018.12.011
在一项新的研究中,来自美国加州大学旧金山分校的研究人员首次证实他们开发出的一种技术诱导多能干细胞---它们能够产生体内的每种细胞类型,并且可在实验室里无限制地生长---产生能够杀死肿瘤细胞的成熟T细胞。这种技术使用一种称为人工胸腺类器官(thymic organoids)的三维结构。这种人工胸腺类器官通过模拟胸腺环境发挥作用。在胸腺中,T细胞是由造血干细胞产生的。相关研究结果于2019年1月17日在线发表在Cell Stem Cell期刊上,论文标题为“Organoid-Induced Differentiation of Conventional T Cells from Human Pluripotent Stem Cells”。论文通讯作者为加州大学旧金山分校的Gay Crooks博士。

在人工胸腺类器官中,人胚胎干细胞产生T细胞(红色轮廓),图片来自UCLA Broad Stem Cell Research Center/Cell Stem Cell。
T细胞是抵抗感染的免疫系统细胞,但也有消除癌细胞的潜力。通过使用加州大学旧金山分校开发出的这种技术让自我更新的多能干细胞产生T细胞的能力可能导致人们开发出新的癌症免疫疗法,并可能促进人们进一步研究针对HIV等病毒感染和自身免疫疾病的T细胞疗法。这种技术最有希望的一个方面是它可以与基因编辑方法相结合,以便创造出几乎无限制的T细胞供应用于大量患者体内而无需使用患者自己的T细胞。
这项新的研究证实人工胸腺类器官能够让目前用于研究的两种多能性干细胞高效地产生成熟的T细胞。这两种多能干细胞是胚胎干细胞,来自于捐赠的胚胎;诱导性多能干细胞,是通过让成体皮肤细胞或血细胞经过重编程后返回到一种胚胎样状态而产生的。
这些研究人员还证实他们能够对多能干细胞进行基因改造,让它们表达一种靶向癌症的T细胞受体,并且利用人工胸腺类器官,让它们产生能够在小鼠体内靶向和杀死肿瘤细胞的T细胞。
6.Nat Commun:如何维持胚胎干细胞的无限潜能?
doi:10.1038/s41467-018-07528-9
近日,一项刊登在国际杂志Nature Communications上的研究报告中,来自索尔克研究所的科学家们通过研究开发了一种新型蛋白复合体,其能抑制干细胞的发展,从而使其能够维持无限的潜能;这种名为GBAF的复合体或有望作为后期科学家们开发新型再生医学疗法的潜在靶点。
研究者Diana Hargreaves教授表示,这项研究中,我们始于对胚胎干细胞多能性的探索,这种多能性能够促进胚胎干细胞转化成为机体中任何一种类型的细胞,阐明控制干细胞多潜能性的多种基因网络非常重要,因此能够找到一种在这一调节过程中扮演关键角色的未知蛋白,对于研究者而言也是非常有意义的。机体中的每一个细胞都有着相同的一套DNA元件,其包含有制造每一种可能性细胞类型的指令;大型的蛋白复合体(染色质重塑器)能够激活或沉默基因的表达,指导胚胎干细胞进入到一种特殊的路径中,就好比一群计划装修房子的承包商们,这些蛋复合体也包含有多重亚单位,不同亚单位的组合就能够改变DNA的物理形状,并且决定哪些基因能够指挥干细胞分化成为肺部细胞或大脑细胞。
文章中,研究人员想通过研究深入理解这些亚单位的聚集方式以及特殊的亚单位如何指挥蛋白复合体的功能,因此研究人员转向对一种名为BRD9的蛋白进行研究,该蛋白与BAF染色质重塑器家族有关,他们推测该蛋白或是其中的一种亚单位;随后研究者将BRD9化学抑制剂应用于胚胎干细胞中,并进行了一系列实验来全面分析与BAF复合体活性改变相关的细胞多潜能性。
研究者发现,BRD9能扮演胚胎干细胞发育制动器的角色,当BRD9开始发挥作用时,细胞就会维持多潜能性,而当BRD9的活性被抑制时,细胞就会开始发育的下一个阶段,随后研究者鉴别出了哪种BAF复合体能在细胞中发挥作用,结果表明,BRD9或许是一种未知BAF复合体的一部分。
7.Int J Mol Sci:转基因小鼠胚胎干细胞中Hes1和Msx1的激活增加成神经嵴衍生物的表达
doi:10.3390/ijms19124025
神经嵴(NC)包括多能细胞群,其产生外周神经元,软骨和平滑肌细胞,以及其他表型。当在经历NC分化的小鼠胚胎干细胞(mESC)中表达时,Hes1和Msx1的作用尚未可知。
在这项工作中,我们生成稳定的mESCs转染编码嵌合蛋白的构建体,其中糖皮质激素受体(GR)的配体结合域,通过加入地塞米松转移到细胞核,与Hes1(HGR)或Msx1(MGR)融合,以及双转基因细胞(HGR + MGR)。这些品系继续表达多能性标志物。在NC分化时,所有品系显示出明显的Sox2表达降低和Sox9,Snai1和Msx1的表达上调,表明NC定型。加入地塞米松以诱导嵌合蛋白的核转位。我们发现胶原IIa转录物在MGR细胞中增加,而HGR + MGR的共激活导致平滑肌肌动蛋白(α-Sma)转录物的显著增加。免疫染色显示HGR + MGR细胞中的活化诱导了更高比例的β-TUBULIN III +,α-SMA +和COL2A1 +细胞。
总之,这些发现表明单独或与HES-1组合的MSX-1的核转位产生软骨细胞样细胞,并且同时激活HES-1和MSX-1增加平滑肌和神经元细胞的产生。
8.Blood:通过抑制PAPD5调节TERC的转录后修饰可恢复角化不良患者的终末造血
doi:10.1182/blood-2018-11-885368
TERC(端粒酶RNA的组成成分)水平降低可导致携带TERC、PARN、NOP10、NHP2、NAF1或DKC1突变的患者发生角化障碍(DC)。抑制非经典poly(A)聚合酶PAPD5或外泌体RNA降解复合物,可部分恢复DKC1突变细胞的TERC水平,但仍不明确TERC的转录后加工的调控是否可改善角化障碍患者的造血输出。
Wilson Chun Fok等人采用一种携带常见角化不良蛋白突变(DKC1_A353V,该突变可导致端粒酶维持功能缺陷和终末造血潜能降低)的人胚胎干细胞(hESCs),来研究EXOSC3活性降低或PAPD5介导的寡腺苷化沉默对DC患者造血祖细胞功能的影响。
DKC1突变型hESCs的EXOSC3或PAPD5水平降低可功能性改善TERC水平和端粒酶活性,并伴随端粒延长和DNA损伤信号的降低。沉默PAPD5,可明显恢复DKC1突变细胞的终末造血潜能,但沉默EXOSC3无此效果。此外,研究人员还发现在分化的CD34+细胞中,PAPD5的抑制作用是持续的,伴随成熟的、功能性的TERC形成增多,提示上调PAPD5可能是逆转DC患者造血功能障碍的一种潜在策略。
9.Nat Commun:蜂王浆蛋白Royalactin能维持干细胞多能性
doi:10.1038/s41467-018-06256-4

图片来自Nature Communications, 2018, doi:10.1038/s41467-018-06256-4。
蜂王浆是蜜蜂Apis mellifera的蜂后制造者,对哺乳动物的长寿、生育和再生具有跨物种效应。尽管有这些知识,人们对蜂王浆或它的组分如何发挥其无数的作用仍然是知之甚少。在一项新的研究中,以小鼠胚胎干细胞(ESC)为平台,美国斯坦福大学的研究人员报道,蜂王浆通过它的主要蛋白组分Royalactin激活一种基态的多能性基因网络来维持这些小鼠胚胎干细胞的多能性。他们进一步鉴定出作为Royalactin的一种哺乳动物结构类似物,Regina也在小鼠胚胎干细胞中诱导出一种幼稚样状态(naive-like state)。这揭示出干细胞自我更新的一个重要的先天性程序。这些发现对于理解跨物种的干细胞命运的分子调节具有广泛的意义。
10.Sci Rep:GRG5参与胚胎和神经干细胞的转化
doi:10.1038/s41598-018-31696-9
格劳乔相关基因5(GRG5)是一种多功能蛋白,其与胚胎晚期和出生后小鼠发育有关。在这里,我们通过分析GRG5在干细胞转化决定中的功能来描述GRG5在早期发育阶段中以前未知的作用。
通过功能损失和功能获得方法,我们证明GRG5的消融使胚胎干细胞(ESC)多能状态失调,而其过表达导致自我更新能力增强和癌细胞样特性获得。由过量表达GRG5的胚胎干细胞产生的畸胎瘤的恶性特征揭示了其致癌基因潜力。此外,转录组学分析和细胞分化方法强调GRG5是抑制中内胚层相关基因的多方面信号调节因子。当ESC没有多能性时,GRG5通过Wnt和BMP信号通路抑制促进神经外胚层规范。此外,GRG5通过维持Notch/Hes和Stat3信号通路的活性来促进成纤维细胞的神经元重编程并维持神经干细胞(NSCs)的自我更新。 总之,我们的研究结果表明GRG5在干细胞生物学中具有多效作用,发挥着干细胞因子和神经转化的作用。(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->



